
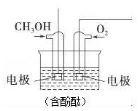
 将甲醇与氧气分别通入如图所示的装置的电极中,可构成甲醇燃料电池,请回答下列问题:
将甲醇与氧气分别通入如图所示的装置的电极中,可构成甲醇燃料电池,请回答下列问题:分析 通入甲醇的电极是负极,反应时该电极反应:CH3OH+8OH--6e-=CO32-+6H2O,故溶液红色变浅;该燃料电池工作时,阳离子向正极移动,电解质溶液为碱性,所以电池正极的电极反应式为:O2+2H2O+4e-=4OH-;根据电路中转移电子相等计算消耗氧气的量.
解答 解:通入甲醇的电极是负极,反应时该电极反应为:CH3OH+8OH--6e-=CO32-+6H2O,故溶液红色变浅;该燃料电池工作时,阳离子向正极移动,即溶液中K+向正极移动,氧气在碱性电解质溶液中得电子,所以电池正极的电极反应式为:O2+2H2O+4e-=4OH-,电池工作过程中通过2mol电子,则理论上消耗O2的体积=$\frac{2mol}{4}$×22.4L/mol=11.2L
故答案为:负;溶液红色变浅;正;O2+2H2O+4e-=4OH-;11.2.
点评 本题考查了原电池原理,涉及电极反应式的书写、离子移动及其转移电子数的计算等知识点,难点是电极反应式的书写,题目难度中等.


 优等生题库系列答案
优等生题库系列答案科目:高中化学 来源: 题型:选择题
| A. | 化学反应必伴随能量变化 | |
| B. | 反应是放热还是吸热取决于反应物和生成物具有的总能量的相对大小 | |
| C. | 可燃物燃烧和酸碱中和反应都是典型的放热反应 | |
| D. | 燃煤发电不需经过其它能量转换过程,可直接把化学能转化为电能 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
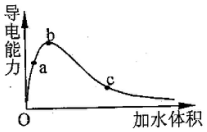
| A. | a,b,c三点溶液的pH:a>b>c | |
| B. | 若用湿润的pH试纸测试c处溶液的pH,比实际的pH偏小 | |
| C. | a,b,c三点溶液用1mol•L-1的NaOH溶液中和,消耗NaOH溶液的体积a>b>c | |
| D. | a,b,c点醋酸的电离程度:c>b>a |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3CH=CHCH3分子中的四个碳原子在同一直线上 | |
| B. | 按系统命名法, 的名称为4,4-二甲基-3-乙基己烷 的名称为4,4-二甲基-3-乙基己烷 | |
| C. | 满足分子式为C4H8ClBr的有机物有11种 | |
| D. | 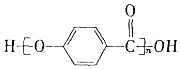 的结构中含有酯基 的结构中含有酯基 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
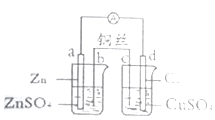
| A. | 电路中电子的流动方向:a-d-CuSO4(aq)一c一b | |
| B. | 该原电池原理:Zn+CuSO4═ZnSO4+Cu | |
| C. | c电极质量减少量等于d电极质量增加量 | |
| D. | d电极反应:Cu2++2e-=Cu,反应后CuSO4溶液浓度下降 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应达到平衡状态时A的转化率为60% | |
| B. | x=4 | |
| C. | 反应达到平衡状态时,相同条件下容器内气体的压强与起始时压强比为6:5 | |
| D. | 若混合气体的密度不再变化,则该可逆反应达到化学平衡状态 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,1.12 L戊烷所含共价键数目为0.8NA | |
| B. | 1 L 0.1 mol/L (NH4)2SO4溶液中含N原子数为0.2NA | |
| C. | 2.2 gD218O与T2O的混合物中所含质子数、中子数均为NA | |
| D. | 一定量的浓硫酸与足量锌共热,产生22.4L气体时,转移的电子数一定为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下是气体 | B. | 能使溴的四氯化碳溶液褪色 | ||
| C. | 不能使酸性高锰酸钾溶液褪色 | D. | 在一定条件下能够聚合生成聚乙烯 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com