
某含Cr2O72- 的含铬废水用硫亚铁铵[(NH4)2 SO4·FeSO4·6H2O]处理,反应中铁元素和
铬元素(+3价)完全转化为沉淀。该沉淀干燥后得到n molFeO·FeyCrxO3 。不考虑处理过
程中的实际损耗,下列叙述错误的是:
A.消耗硫酸亚铁铵的物质量为n(2-x)mol B.处理废水中Cr2O72- 的物质的量为 mol
C.反应中发生转移的电子数为3nx mol D.在FeO·FeyCrxO3中3x=y
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:阅读理解

| NaOH |
| Cl2 |
| 酸化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、反应中转移的电子总数为3nx mol | B、Cr2O72-转化为沉淀时被氧化 | C、消耗硫酸亚铁铵的物质的量为n(2-x)mol | D、在FeO?FeyCrxO3中3y=x |
查看答案和解析>>
科目:高中化学 来源:2013-2014学年湖北省孝感市三年级第一次统一考试化学试卷(解析版) 题型:选择题
某含Cr2O72-废水用硫酸亚铁铵[(NH4)2 Fe(SO4)2•6H2O]处理,反应中铁元素和铬元素完全转化为沉淀。该沉淀干燥后得到n molFeO·FeyCrxO3。不考虑处理过程中的实际损耗,下列叙述正确的是
A.反应中转移的电子总数为3nx mol
B.Cr2O72-转化为沉淀时被氧化
C.消耗硫酸亚铁铵的物质的量为n(2-x)mol
D.在FeO•FeyCrxO3中3y=x
查看答案和解析>>
科目:高中化学 来源:2011-2012学年北京市丰台区高三(上)期末化学试卷(解析版) 题型:解答题
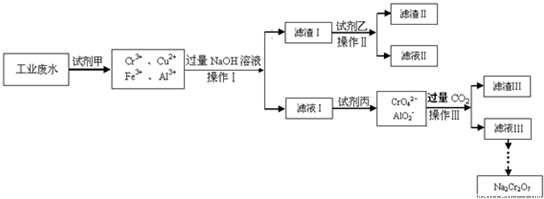
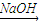 NaCrO2
NaCrO2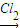 Na2CrO4
Na2CrO4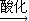 Na2Cr2O7
Na2Cr2O7查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com