
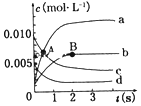
 ��2L�ܱ������У�800��ʱ��Ӧ2NO��g��+O2��g��?2NO2��g����ϵ�У�n��NO�� ��ʱ��ı仯�����
��2L�ܱ������У�800��ʱ��Ӧ2NO��g��+O2��g��?2NO2��g����ϵ�У�n��NO�� ��ʱ��ı仯�����| ʱ��/s | 0 | 1 | 2 | 3 | 4 | 5 |
| n��NO��/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
���� ��1��ƽ�ⳣ������������ƽ��Ũ�ȵ��ݴη��˻����Է�Ӧ��ƽ��Ũ�ȵ��ݴη��˻�����֪��K��300�棩��K��350�棩���¶�Խ��ƽ�ⳣ��ԽС������ƽ��������У�
��2���ɱ������ݿ�֪��3s��ʼ��NO�����ʵ���Ϊ0.007mol�����ٱ仯��3sʱ��Ӧ��ƽ�⣬NO2�Dz���淴Ӧ����Ũ������ƽ��ʱŨ��ΪNOŨ�ȵı仯����c��NO����
����v=$\frac{��c}{��t}$����v��NO��������������֮�ȵ��ڻ�ѧ������֮�ȼ���v��O2����
��3�����淴Ӧ�ﵽƽ��ʱ��v��=V�� ��ͬ�����ʱ�ʾ������������֮�ȵ��ڻ�ѧ������֮�ȣ���ͬ���ʱ�ʾ������Ӧ��������ֵ����ʵ�����Ũ�ȡ��������ٱ仯���Լ��ɴ�������һЩ��Ҳ�������仯��ע��ѡ���ж�ƽ���������Ӧ�淴Ӧ���з����仯�����������ɱ仯�����仯��˵����Ӧ����ƽ�⣻
��4��Ϊʹ�÷�Ӧ�ķ�Ӧ�������ɲ�������ѹǿ�������¶ȡ��������������Ӧ��Ũ�ȵȷ������ٽ��ƽ���ƶ�ԭ���������
��5��ƽ�ⳣ��ֻ���¶ȱ仯��
��� �⣺��1��2NO��g��+O2��g��?2NO2��g������Ӧ��ƽ�ⳣ��K=$\frac{{c}^{2}��N{O}_{2}��}{{c}^{2}��NO��c��{O}_{2}��}$������ƽ�������ȷ�Ӧ������У���֪��K��300�棩��K��350�棩���¶�Խ��ƽ�ⳣ��ԽС������ƽ��������У��������ӦΪ���ȷ�Ӧ��
�ʴ�Ϊ��$\frac{{c}^{2}��N{O}_{2}��}{{c}^{2}��NO��c��{O}_{2}��}$�����ȣ�
��2���ɱ������ݿ�֪��3s��ʼ��NO�����ʵ���Ϊ0.007mol�����ٱ仯��3sʱ��Ӧ��ƽ�⣬NO2�Dz���淴Ӧ����Ũ������ƽ��ʱŨ��ΪNOŨ�ȵı仯����c��NO��=$\frac{0.02mol-0.007mol}{2L}$=0.0065mol/L������ͼ�б�ʾNO2�仯��������b��
2s����NO��ʾ��ƽ����Ӧ����v��NO��=$\frac{\frac{��n}{V}}{��t}$=$\frac{\frac{0.02mol-0.008mol}{2L}}{2s}$=3.0��10-3mol•L-1•s-1������֮�ȵ��ڻ�ѧ������֮�ȣ�����v��O2��=$\frac{1}{2}$v��NO��=$\frac{1}{2}$��3.0��10-3mol•L-1•s-1=1.5��10-3mol•L-1•s-1��
�ʴ�Ϊ��b��1.5��10-3mol•L-1•s-1��
��3��a��δָ���������ʣ�������ʾͬһ����Ӧ���ʣ�v��NO2����ʼ����Ϊv��O2����2��������˵���ﵽƽ�⣬��a����
b������������䣬�淴Ӧ���У���Ӧ��������ܵ����ʵ����ڼ�С��������ѹǿ��С����������ѹǿ���ֲ��䣬˵����Ӧ����ƽ�⣬��b��ȷ��
c����ͬ���ʱ�ʾ���ʣ�����ƽ��ʱ����������֮�ȵ��ڻ�ѧ������֮�ȣ�V�� ��NO��������O2��=2��1����V�� ��NO��=2v����O2������c��ȷ��
d�������������������䣬�����ݻ�Ϊ��ֵ�������ܶ���ʼ���ղ��䣬����˵���ﵽƽ�⣬��d����
�ʴ�Ϊ��bc��
��4��a����ʱ�����NO2����ƽ�������ƶ�������Ӧ���ʼ�С���ʴ���
b���ʵ������¶ȣ���Ӧ��������ƽ�����淴Ӧ�����ƶ����ʴ���
c������O2��Ũ�ȷ�Ӧ���������Ҹ÷�Ӧ������Ӧ�����ƶ�������ȷ��
d��ѡ���Ч����������Ӧ���ʣ���ƽ�ⲻ�ƶ����ʴ���
��ѡc��
�ʴ�Ϊ��c��
��5���������������С��1L��ѹǿ����ƽ�ⳣ�����¶ȱ仯����Ӧ�ﵽƽ��ʱ��ƽ�ⳣ�����䣬
�ʴ�Ϊ�����䣮
���� ���⿼�����ʵ���Ũ����ʱ��仯���ߡ���Ӧ���ʼ��㡢ƽ��ƽ��״̬���жϣ��Ѷ��еȣ��ж�ƽ��ʱҪע�⣬ѡ���жϵ������������ŷ�Ӧ�Ľ��з����仯�������������ɱ仯����ֵʱ��˵�����淴Ӧ����ƽ��״̬��


 �п�������㾫��ϵ�д�
�п�������㾫��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
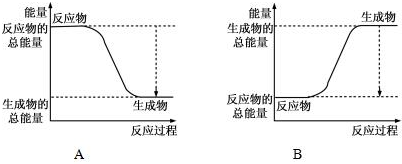
| ��ѧ�� | H-H | O=O | H-O |
| ����kJ/mol | 436 | 496 | 463 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����C���� | |
| B�� | �Ӵ��� | |
| C�� | ����������䣬���뵪��ʹ��ϵѹǿ���� | |
| D�� | ����ѹǿ���䣬���뵪��ʹ����������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
 �¶�ΪTʱ����2.0L�����ܱ������г���1.0mol PCl5����ӦPCl5��g�� PCl3��g��+Cl2��g������һ��ʱ���ﵽƽ�⣮��Ӧ�����вⶨ��n��PCl3����ʱ��ı仯��ͼ������˵����ȷ���ǣ�������
�¶�ΪTʱ����2.0L�����ܱ������г���1.0mol PCl5����ӦPCl5��g�� PCl3��g��+Cl2��g������һ��ʱ���ﵽƽ�⣮��Ӧ�����вⶨ��n��PCl3����ʱ��ı仯��ͼ������˵����ȷ���ǣ�������| A�� | ��Ӧ��ǰ50 s ��ƽ������v��PCl5��=0.0032 mol•L-1•s-1 | |
| B�� | �÷�Ӧ��ƽ�ⳣ��K=0.025 | |
| C�� | ��ͬ�¶��£���ʼʱ�������г���1.0 mol PCl5��0.20molPCl3 ��0.20 mol Cl2����Ӧ�ﵽƽ��ǰv��������v���棩 | |
| D�� | ���������������䣬�����¶ȣ�ƽ��ʱ��c��PCl3��=0.11mol•L-1����Ӧ�ġ�H��0 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Fe | B�� | SO2 | C�� | KMnO4 | D�� | Ũ H2SO4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��Ʒ����Һ��ͨ������X��Ʒ����Һ��ɫ��������X������Cl2 | |
| B�� | CO2�к�����SO2���ɽ��û������ͨ����������NaHCO3��Һ�г�ȥSO2�� | |
| C�� | �ýྻ�IJ�˿պȡijʳ���������ھƾ��ƻ��������գ������Ի�ɫ��˵����ʳ�������в���KIO3 | |
| D�� | ��ͬ�����pH��Ϊ3��HA��HB���������Һ�ֱ���������п��ַ�Ӧ��HA�ų��������࣬˵��HB�����Ա�HA������ǿ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com