
| A. | 用托盘天平称量时,将NaOH固体放在左盘内的纸上,称得质量为10.2 g | |
| B. | 用25 mL碱式滴定管量取高锰酸钾溶液,体积为16.60 mL | |
| C. | 用广泛pH试纸测稀盐酸的pH=3.2 | |
| D. | 用10 mL量筒量取NaCl溶液,体积为9.2 mL |
分析 A.NaOH易潮解且具有强腐蚀性;
B.碱式滴定管只能量取碱性溶液;
C.广泛pH试纸的测定值是整数;
D.量筒的感量是0.1mL,量取溶液时量筒规格要等于或稍微大于量取溶液体积.
解答 解:A.NaOH易潮解且具有强腐蚀性,所以NaOH应该放置在小烧杯中称量,故A错误;
B.碱式滴定管只能量取碱性溶液,酸性高锰酸钾溶液呈酸性,要用酸式滴定管量取,故B错误;
C.广泛pH试纸的测定值是整数,所以用广泛pH试纸测稀盐酸的pH不能为3.2,故C错误;
D.量筒的感量是0.1mL,量取溶液时量筒规格要等于或稍微大于量取溶液体积,所以用10 mL量筒量取NaCl溶液,体积为9.2 mL,故D正确;
故选D.
点评 本题考查化学实验方案评价,为高频考点,涉及仪器选取、物质称量等知识点,明确仪器用途、仪器感量、基本实验操作等知识点即可解答,注意含有刻度仪器的感量,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 根据上述热化学方程式可以确定H2、CH4的燃烧热 | |
| B. | H2(g)+$\frac{1}{2}$O2(g)═H2O(1)△H=-241.8kJ•mol-1 | |
| C. | CH4(g)+$\frac{3}{2}$O2(g)═CO(g)+2H2O(g)△H>-890.31kJ•mol-1 | |
| D. | 8gCH4完全燃烧释放出的热量为445.155kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
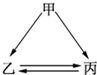 如图所示的甲、乙、丙三种物质均含有相同的某种元素,箭头表示物质间的转化一步就能实现,则甲可能是( )
如图所示的甲、乙、丙三种物质均含有相同的某种元素,箭头表示物质间的转化一步就能实现,则甲可能是( )| A. | ①②③⑤ | B. | ②③④⑤ | C. | ①②③④ | D. | ①②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 生铁中含有碳,抗腐蚀能力比纯铁强 | |
| B. | 钢铁发生析氢腐蚀时,负极反应是:Fe-3e-═Fe3+ | |
| C. | 在铁制品上镀铜时,镀件为阳极,铜盐为电镀液 | |
| D. | 铁管上镶嵌锌块,铁管不易被腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
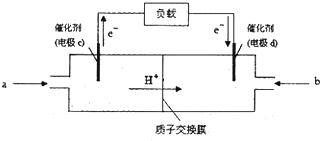
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | XeF4分子具有非常好的热稳定性 | |
| B. | XeF4分子中Xe的化合价为0价 | |
| C. | 氧化剂和还原剂的物质的量之比为2:3 | |
| D. | 每生成4molXe转移16mol电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含有AgCl和AgI固体的悬浊液:c(Ag+)>c(C1-)=c(I-) | |
| B. | CO2的水溶液:c(H+)>c(HCO3-)═2c(CO32-) | |
| C. | pH=1的NaHSO4溶液:c(H+)=c(SO42-)十c(OH-) | |
| D. | 含等物质的量的NaHC2O4和Na2C2O4的溶液:3c(Na+)═2[c(HC2O4-)+c(C2O42-)+c(H2C2O4)] |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
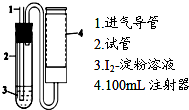 二氧化硫是造成大气污染的主要有害气体之一,某合作学习小组的同学拟测定某地大气中SO2的含量,实验步骤及装置如下:
二氧化硫是造成大气污染的主要有害气体之一,某合作学习小组的同学拟测定某地大气中SO2的含量,实验步骤及装置如下:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com