
 £Ø1£©ŅŃÖŖŌŚ³£ĪĀ³£Ń¹ĻĀ£ŗ
£Ø1£©ŅŃÖŖŌŚ³£ĪĀ³£Ń¹ĻĀ£ŗ·ÖĪö £Ø1£©ĄūÓĆøĒĖ¹¶ØĀÉ£¬½«¢Ł”Į$\frac{1}{2}$-¢Ś”Į2æÉµĆ¼×“¼Č¼ÉÕČȵÄČČ»Æѧ·½³ĢŹ½£»
£Ø2£©·“Ó¦µÄģŹ±ä=·“Ó¦Īļ¶ĻĮŃ»Æѧ¼üĪüŹÕµÄÄÜĮæ-Éś³ÉĪļŠĪ³É»Æѧ¼ü·Å³öµÄÄÜĮ棬½įŗĻĶ¼Ļó¼ĘĖć½ā“š£®
½ā“š ½ā£ŗ£Ø1£©±ķŹ¾¼×“¼µÄČ¼ÉÕČȵĻÆѧ·½³ĢŹ½£¬Ó¦ŹĒ1mol¼×“¼·“Ó¦£¬ĒŅÉś³É¶žŃõ»ÆĢ¼ŗĶŅŗĢ¬Ė®£¬ĄūÓĆøĒĖ¹¶ØĀÉ£¬½«¢Ł”Į$\frac{1}{2}$-¢Ś”Į2æÉµĆ¼×“¼Č¼ÉÕČȵÄČČ»Æѧ·½³ĢŹ½ĪŖCH3OH£Øl£©+$\frac{3}{2}$O2£Øg£©ØTCO2£Øg£©+2H2O£Øl£©”÷H=-725.8kJ•mol-1£¬
¹Ź“š°øĪŖ£ŗCH3OH£Øl£©+$\frac{3}{2}$O2£Øg£©ØTCO2£Øg£©+2H2O£Øl£©”÷H=-725.8kJ•mol-1£»
£Ø2£©ŅĄ¾ŻĶ¼Ļó·ÖĪö£¬·“Ó¦ĪŖN2H4+O2=N2+2H2O£¬·“Ó¦µÄģŹ±ä”÷H=-534KJ/mol£¬·“Ó¦µÄģŹ±ä=·“Ó¦Īļ¶ĻĮŃ»Æѧ¼üĪüŹÕµÄÄÜĮæ-Éś³ÉĪļŠĪ³É»Æѧ¼ü·Å³öµÄÄÜĮ棬Éč¶ĻĮŃ1molN-H¼üĪüŹÕµÄÄÜĮæĪŖx£¬¶ĻĮŃ»Æѧ¼üĪüŹÕµÄÄÜĮæ=2752-534=2218£¬ŠĪ³ÉŠĀ¼üŹĶ·ÅµÄÄÜĮæ=4x+154+500=2752-534£¬½āµĆ£ŗx=391£¬
¹Ź“š°øĪŖ£ŗ391£®
µćĘĄ ±¾Ģāæ¼²éČČ»Æѧ·½³ĢŹ½µÄŹéŠ“£¬ĪŖøßĘµæ¼µć£¬²ąÖŲæ¼²éѧɜµÄ·ÖĪöÄÜĮ¦ŗĶ¼ĘĖćÄÜĮ¦£¬ĢāÄæÄѶČÖŠµČ£¬×¢Ņā°ŃĪÕģŹ±ä¼ĘĖć·½·ØŹĒ½āĢā¹Ų¼ü£®


 ĆūŠ£æĪĢĆĻµĮŠ“š°ø
ĆūŠ£æĪĢĆĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Č¼ĆŗÖŠ¼ÓČĖÉśŹÆ»ŅæɽµµĶŗ¬Įņ»ÆŗĻĪļµÄÅÅ·Å | |
| B£® | æÉÓƵķ·ŪČÜŅŗ¼ģŃéŹ³ŃĪÖŠŹĒ·ń¼Óµā | |
| C£® | Äš¾Ę¹¤ŅµÖŠŹ¹ÓƵĔ°¾ĘĒś”±ŹĒŅ»ÖÖĆø | |
| D£® | æÉÓĆÕōĮó·Ø”¢µēÉųĪö·Øµ»Æŗ£Ė® |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¼ĘĖćĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
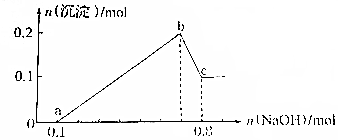 ijČÜŅŗÖŠæÉÄÜŗ¬ÓŠH+”¢Mg2+”¢Al3+”¢Fe3+”¢Na+µČŃōĄė×ÓÖŠµÄŅ»ÖÖ»ņ¼øÖÖ£¬µ±ĻņøĆČÜŅŗÖŠ¼ÓČėNaOHČÜŅŗŹ±£¬²śÉś³ĮµķµÄĪļÖŹµÄĮæÓėĖł¼ÓNaOHĪļÖŹµÄĮæÖ®¼äµÄ¹ŲĻµČēĶ¼ĖłŹ¾
ijČÜŅŗÖŠæÉÄÜŗ¬ÓŠH+”¢Mg2+”¢Al3+”¢Fe3+”¢Na+µČŃōĄė×ÓÖŠµÄŅ»ÖÖ»ņ¼øÖÖ£¬µ±ĻņøĆČÜŅŗÖŠ¼ÓČėNaOHČÜŅŗŹ±£¬²śÉś³ĮµķµÄĪļÖŹµÄĮæÓėĖł¼ÓNaOHĪļÖŹµÄĮæÖ®¼äµÄ¹ŲĻµČēĶ¼ĖłŹ¾²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŌŚæÕĘųÖŹĮæČÕ±ØÖŠCO2ŗ¬ĮæŹōÓŚæÕĘųĪŪČ¾ÖøŹż | |
| B£® | ČÕ³£Éś»īÖŠŗĶŅ½Ōŗ³£ÓĆĪŽĖ®ŅŅ“¼É±¾śĻū¶¾ | |
| C£® | ĀĢÉ«Ź³Ę·ŹĒÖø²»ŗ¬ČĪŗĪ»ÆѧĪļÖŹµÄŹ³Ę· | |
| D£® | ÄæĒ°¼ÓµāŹ³ŃĪÖŠÖ÷ŅŖĢķ¼ÓµÄŹĒKIO3 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ½«·Ļ¾Éµē³Ų¼ÆÖŠÉīĀń£¬·ĄÖ¹ÖŲ½šŹōĪŪČ¾ | |
| B£® | øÄÉĘÄÜŌ“½į¹¹£¬“óĮ¦·¢Õ¹Ģ«ŃōÄÜ”¢·ēÄܵČĒå½ąÄÜŌ“ | |
| C£® | ĶĘ¹ćĢ¼²¶¼ÆŗĶ×Ŗ»Æ³É»Æ¹¤ŌĮĻ¼¼Źõ£¬Öš²½ŹµĻÖ¶žŃõ»ÆĢ¼ĮćÅÅ·Å | |
| D£® | ²ÉÓĆÄÉĆ×TiO2¹ā“„Ć½¼¼Źõ£¬½«×°ŠŽ²ÄĮĻÖŠŹĶ·ÅµÄHCHO×Ŗ»ÆĪŖĪŽŗ¦ĪļÖŹ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | CaO | B£® | Na2CO3 | C£® | SiO2 | D£® | CaCO3 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
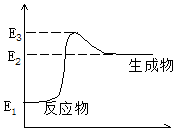 C£Øs£©+H2O£Øg£©”śCO£Øg£©+H2£Øg£©+Q£¬·“Ó¦¹ż³ĢÖŠÄÜĮæ£ØE£©µÄ±ä»ÆČēĶ¼ĖłŹ¾£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©
C£Øs£©+H2O£Øg£©”śCO£Øg£©+H2£Øg£©+Q£¬·“Ó¦¹ż³ĢÖŠÄÜĮæ£ØE£©µÄ±ä»ÆČēĶ¼ĖłŹ¾£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©| A£® | ¼õŠ”Ń¹ĒæŹ±£¬QµÄÖµŌö“ó | B£® | ÉżøßĪĀ¶ČŹ±£¬QµÄÖµ¼õŠ” | ||
| C£® | øĆ·“Ó¦ŹĒĪüČČ·“Ó¦ | D£® | Q=E3-E1 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com