
����Ŀ����ҵ������������Ҫ�ɷ�ΪAl2O3 �� ֻ��Fe2O3���ʣ�Ϊԭ��ұ�����Ĺ����������£�
�ش��������⣺
��1��ʵ���ҽ��й����õ��IJ����������ձ����������� ��
��2��������Ӧ�Ƿ���������ԭ��Ӧ����ǡ�����д����Ӧ�ٵĻ�ѧ����ʽ ��
��3����Ӧ�ٺ���˵ij���Ϊ �� ����ȷ���������н���Ԫ�ؼ����̬�IJ������� ��
��4���������Ƶõ�þ���Ͻ���;�ܹ㷺�����������ֻ�������ij����С������ijһƷ���ֻ���������þ�Ͻ�����о����ⶨ��������������������������
I�������������ᡢ����������Һ�������ʵ�鷽����
��������þ�Ͻ� ![]() ��Һ
��Һ ![]()
![]() �������ղ�����������ø÷�������ʵ��ʱ�����˳������ղ���������⣬����������� ��
�������ղ�����������ø÷�������ʵ��ʱ�����˳������ղ���������⣬����������� ��
II����չ�о���������þ�Ͻ�������������Һ�м������NaOH��Һʱ�����ɳ��������������NaOH��Һ����Ĺ�ϵ���������ϵ��ʾ��
������60��70ml����������Һʱ����д�����������ӷ���ʽ �� ���жϣ�����ͼ�����е������ܷ�����Ͻ�������������������ѡ��ܡ����ܡ�����
���Т٢�����ѡһ�����𣮣�����֣�
������������Ͻ�������������������˵�����ɣ�
����������Ͻ�������������������������������Ϊ ��
���𰸡�
��1��©��
��2����Al2O3+2NaOH=2NaAlO2+H2O
��3��Fe2O3��ȡ����������һ֧�ྻ�Թܣ���������ϡ���ᣨ�����ᣩʹ����ȫ�ܽ⣬�ٵμ��������軯�أ������軯泥�������Һ�ʣ�Ѫ����ɫ��˵����ΪFe2O3
��4���Ͻ���Ʒ��������Al��OH��3+2OH��=2AlO ![]() +H2O���ܣ�52.94%
+H2O���ܣ�52.94%
���������⣺��1��ʵ���ҽ��й����õ��IJ����������ձ�����������©�������Դ��ǣ�©������2��������Ӧ�з�Ӧ�٢ڢ۶��Ƿ�������ԭ��Ӧ����Ӧ��Ϊ���������������Ʒ�Ӧ����ƫ�����ƺ���������Ӧ�Ļ�ѧ����ʽΪ�����Դ��ǣ���Al2O3+2NaOH=2NaAlO2+H2O����3����������ķ�����֪����Ӧ�ٺ���˵ij���ΪFe2O3 �� Ҫȷ���������н���Ԫ�ؼ����̬�����������ܽ⣬����KSCN��Һ���������ӵĴ��ڣ���������Ϊ�����Դ��ǣ�Fe2O3��ȡ����������һ֧�ྻ�Թܣ���������ϡ���ᣨ�����ᣩʹ����ȫ�ܽ⣬�ٵμ��������軯�أ������軯泥�������Һ�ʣ�Ѫ����ɫ��˵����ΪFe2O3����4��I�����յõ���������þ������Ҫ����Ͻ���þ����������������Ҫ�����Ͻ���Ʒ�����������Դ��ǣ��Ͻ���Ʒ��������II��������60��70ml����������Һʱ��������������С���������������������Ʒ�����Ӧ������ƫ�����ƣ���Ӧ�����ӷ���ʽΪAl��OH��3+2OH��=2 AlO ![]() +H2O�����������֪���ܽ������������ĵ�����������Һ��70ml��60ml=10ml�������������������ĵ�����������Һ���Ӧ����30ml����������������þ���ĵ�����������Һ�����60ml��10ml��30ml=20ml������ݷ���ʽMg2++2OH��=Mg��OH��2����Al3++3OH��=Al��OH��3����֪Al��Mg�����ʵ���֮����1��1�ģ�����������������
+H2O�����������֪���ܽ������������ĵ�����������Һ��70ml��60ml=10ml�������������������ĵ�����������Һ���Ӧ����30ml����������������þ���ĵ�����������Һ�����60ml��10ml��30ml=20ml������ݷ���ʽMg2++2OH��=Mg��OH��2����Al3++3OH��=Al��OH��3����֪Al��Mg�����ʵ���֮����1��1�ģ����������������� ![]() =52.94%��
=52.94%��
���Դ��ǣ�Al��OH��3+2OH��=2 AlO ![]() +H2O���ܣ�52.94%��
+H2O���ܣ�52.94%��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ�鷽���в��ܴﵽ��Ӧʵ��Ŀ���ǣ� ��
A | B | C | D | |
���� |
|
|
|
|
Ŀ�� | ̽��Ũ�ȶԻ�ѧ��Ӧ���ʵ�Ӱ�� | �Ʊ����� | �����±Ƚ�NaHCO3��Na2CO3���ܽ�� | ̽���¶ȶԻ�ѧƽ���Ӱ�� |
A.A
B.B
C.C
D.D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ϳɰ�������ع�ҵ�У��������ʼ��ת����ϵ��ͼ������˵������ȷ���ǣ� ��
A.�ס��ҡ������������ж����е�Ԫ��
B.��ӦII��III�͢����������ֱ��������������Ͷ�����������һ��
C.����������ˮ֮�䷴Ӧ���������NO��VI�IJ���NO�������������б��ٴ�����
D.�����Ͷ�����̼ͨ���Ȼ�����Һ���������ܽ�Ƚ�С��̼�����ƾ��壬������Ӧ��NH3+CO2+H2O+NaCl�TNaHCO3��+NH4Cl
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������к��е������ᣨ��ṹ��ʽ���£�������ƻ�����нϺõı���Ч����������һ��ʱ���ڷ�ֹ����ƻ�������ɫ������˵������ȷ���ǣ� �� 
A.������ķ���ʽ��C6H8O7
B.��������������ˮ���л���
C.����������к����Ȼ����ǻ�
D.������ֻ�ܷ���ȡ����Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ԫ��X��Y��Zԭ������֮��Ϊ36��X��Y��ͬһ���ڣ�X����Z2��������ͬ�ĺ�����Ӳ�ṹ������˵������ȷ���ǣ� ��
A. X����Ԫ��B. ���Ӱ뾶X����Z2��
C. ͬ��Ԫ����Z���⻯���ȶ�����ǿD. ͬ����Ԫ����Y�ķǽ�������ǿ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������¶ȣ����г����в�һ��������ǣ�
A. ���볣��Ka B. ��ѧƽ�ⳣ��K
C. ˮ�����ӻ�����Kw D. �ε�ˮ�ⳣ��Kh
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijͬѧ��������ʵ�飺����˵���������ǣ� ��
װ�� | ���� | ���� |
| ��ʢ��Ũ������ձ�A����ʢ�е���KI��Һ���ձ�C�У�Ȼ��ͭƬ�����ձ�A���������ձ�B��ס | �ձ�AҺ���Ϸ��������ִ�������ɫ���壻һ��ʱ�����ɫ������ʧ���ձ�A��C�е�Һ�嶼�����ɫ |
A.�ձ�A�з�����Ӧ��3Cu+8HNO3�T3Cu��NO3��2+2NO��+4H2O
B.����ɫ������ʧֻ��NO2���ձ�C�е�KI������Ӧ�й�
C.�ձ�C����Һ����ֻ��NO2��C����Һ������Ӧ�й�
D.����ͭƬ������Ƭ����C�е�Һ��Ҳ���ܱ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��CO2����Ҫ�Ļ���ԭ�ϣ�Ҳ��Ӧ�ù㷢�Ļ�����Ʒ��CO2��������ƻ������ط�Ӧ�ɲ���������
������м��㣺
��1��CO2ͨ�백ˮ����NH4HCO3 �� NH4HCO3�����ֽ⣮2.00mol NH4HCO3��ȫ�ֽ⣬�ֽ���ᆳ���������ΪL����״������
��2��ijH2�к���2.40molCO2 �� �û������ͨ��2.00L NaOH��Һ�У�CO2����ȫ���գ����NaOH��ȫ��Ӧ����NaOH��Һ��Ũ��Ϊ ��
��3��CO2��KO2�����з�Ӧ��
4KO2+2CO2��2K2CO3+3O2
4KO2+4CO2+2H2O��4KHCO3+3O2
��9mol CO2���ܷ���ں�KO2��Ӧ������9mol O2 �� ��Ӧǰ�ܷ����H2O����Ӧ���Ƕ��٣���ʽ���㣮
��4�������ˮ������Ӧ�IJ����Ǻϳɼ״���ԭ�ϣ�CH4+H2O ![]() CO+3H2 �� ��֪��CO+2H2
CO+3H2 �� ��֪��CO+2H2![]() CH3OH CO2+3H2
CH3OH CO2+3H2![]() CH3OH+H2O��300mol CH4��ȫ��Ӧ��IJ����У�����100mol CO2��ϳɼ״�������ü״�350mol����������120mol������CO2��ת���ʣ�
CH3OH+H2O��300mol CH4��ȫ��Ӧ��IJ����У�����100mol CO2��ϳɼ״�������ü״�350mol����������120mol������CO2��ת���ʣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ�й����ʣ����ɶ�����Ԫ���γɣ�֮���ת����ϵ������AΪ�����Ľ������ʣ�BΪ�ǽ������ʣ�һ���Ǻ�ɫ��ĩ����C�dz�������ɫ��ζҺ�壬D�ǵ���ɫ�Ĺ��廯�������Ӧ����ͼ����ʡ�ԣ� 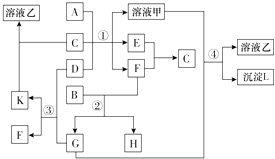
��1��A��B��C��D���������ʷֱ�Ϊ���������ѧʽ����
��2����Ӧ���е�C��D���������÷�Ӧ�Ļ�ѧ����ʽ�� ��
��3����Ӧ�ܵ����ӷ���ʽΪ ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com