
(16分)现用质量分数为98%、密度为1.84 g·cm-3的浓H2SO4来配制500 mL0.25 mol/L的稀H2SO4。
可供选择的仪器有:①玻璃棒 ②烧瓶 ③烧杯 ④胶头滴管 ⑤量筒⑥容量瓶 ⑦托盘天平 ⑧药匙。
请回答下列问题:
(1)上述仪器中,在配制稀H2SO4时用不到的有 (填代号)。
(2)经计算,需浓H2SO4的体积为 。现有①10 mL ②50 mL ③100 mL三种规格的量筒,应选用的量筒是 (填代号)。
(3)将浓H2SO4加适量蒸馏水稀释,冷却片刻,随后全部转移到 mL的容量瓶中,转移时应用玻璃棒 。转移完毕,用少量蒸馏水洗涤 2~3次,并将洗涤液全部转移到容量瓶中,再加适量蒸馏水,振荡容量瓶,使溶液混合均匀。然后缓缓地把蒸馏水直接注入容量瓶直到液面接近刻度处。改用 加蒸馏水到瓶颈刻度的地方,使溶液的 。振荡、摇匀后,装瓶、贴签。
(4)在配制过程中,其他操作都准确,下列操作中:能引起误差偏高的有 (填代号)。
①洗涤量取浓H2SO4后的量筒,并将洗涤液转移到容量瓶中
②未等稀释后的H2SO4溶液冷却至室温就转移到容量瓶中
③将浓H2SO4直接倒入烧杯,再向烧杯中注入蒸馏水稀释浓H2SO4
④定容时,加蒸馏水超过标线,又用胶头滴管吸出
⑤转移前,容量瓶中含有少量蒸馏水
⑥定容摇匀后,发现液面低于标线,又用胶头滴管加蒸馏水至标线
⑦定容时,俯视标线
(1)②⑦⑧ ;(2)6.8mL ,① ;
(3)500 ,引流 ,烧杯和玻璃棒 ,1~2cm,胶头滴管,凹液面与刻度线相切;(4)①②⑦
解析试题分析:(1)配制500 mL0.25 mol/L的稀H2SO4需要使用的仪器有:量筒、烧杯、玻璃棒、500mL容量瓶、胶头滴管,上述仪器中,在配制稀H2SO4时用不到的有②⑦⑧ ;
(2)98%的浓硫酸(其密度为1.84g/cm3)的物质的量浓度为:c=1000×1.84×98%/98=18.4mol/L,配制500mL 0.25mol?L-1稀硫酸,需要浓硫酸的体积为:0.25mol/L×0.5L/18.4mol/L≈0.0068L=6.8mL,应选用10mL的量筒 答案为:6.8mL ,①;
(3)将浓H2SO4加适量蒸馏水稀释,冷却片刻,随后全部转移到500mL的容量瓶中,转移时应用玻璃棒引流。转移完毕,用少量蒸馏水洗涤烧杯和玻璃棒2~3次,并将洗涤液全部转移到容量瓶中,再加适量蒸馏水,振荡容量瓶,使溶液混合均匀。然后缓缓地把蒸馏水直接注入容量瓶直到液面接近刻度1~2cm处。改用胶头滴管加蒸馏水到瓶颈刻度的地方,使溶液的凹液面与刻度线相切,振荡、摇匀后,装瓶、贴签。
(4)①洗涤量取浓H2SO4后的量筒,并将洗涤液转移到容量瓶中,导致溶质增多,所配溶液浓度偏高;②未等稀释后的H2SO4溶液冷却至室温就转移到容量瓶中,导致水加少了,所配溶液浓度偏高;③稀释浓硫酸,需要将浓硫酸慢慢倒入水中,并用玻璃棒不断搅拌,错误;④定容时,加蒸馏水超过标线,又用胶头滴管吸出,导致体积增大,所配溶液浓度偏低,⑤转移前,容量瓶中含有少量蒸馏水,无影响;⑥定容摇匀后,发现液面低于标线,又用胶头滴管加蒸馏水至标线,导致水加多了,所配溶液浓度偏低;⑦定容时,俯视标线 ,导致水加少了,所配溶液浓度偏高,选①②⑦。
考点:考查配制一定物质的量浓度的溶液,误差分析等知识。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:单选题
2005年6月5日我国环境日主题是“人人参与,创建绿色家园”。下列说法不正确的是
| A.回收废旧电池 |
| B.加强控制燃放烟花爆竹法规 |
| C.停止使用含铅汽油 |
| D.将工厂烟囱加高,减少周围大气污染 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
14分)用密度为1.84g/mL,质量分数为98%的浓硫酸配制100 ml 3.0mol/L 稀硫酸的实验步骤如下:①计算所用浓硫酸的体积 ②量取一定体积的浓硫酸 ③稀释 ④转移
⑤洗涤 ⑥定容 ⑦摇匀
(1)所需浓硫酸的体积是 。
(2)第③步实验的操作是 。
(3)第⑥步实验的操作是 。
(4)下列情况对所配制的稀硫酸浓度有何影响?(用字母填写a.偏大 b.偏小 c.无影响)
| A.所用的浓硫酸长时间放置在密封不好的容器中 |
| B.容量瓶用蒸馏洗涤后残留有少量的水 |
| C.所用过的烧杯、玻璃棒未洗涤 |
| D.量取浓硫酸时仰视量筒上的刻度取用浓硫酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
8分)准确称取12 g铝土矿样品(含Al2O3、Fe2O3、SiO2)放入盛有100 mL某浓度硫酸溶液的烧杯中,充分反应后过滤,向滤液中加入10 mol·L-1的NaOH溶液,产生的沉淀质量m与加入的NaOH溶液的体积V的关系如图所示:
请填空回答:
(1)H2SO4溶液的物质的量浓度为_________________。
(2)若a=4.6,用于沉淀Fe3+消耗NaOH的体积是____________mL,铝土矿中各成分的质量分数:Al2O3为______________, SiO2为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
(16分)(1)写出下图中序号①~④仪器的名称:
① ;② ;③ ;④ ;
(2)仪器①~④中,使用前必须检漏的 。(填仪器序号)
(3)分离碘水中的碘应在 (填装置序号)进行 和 操作。
(4)现欲用98%的浓硫酸(密度为1.84g/cm3)配制成浓度为0.5 mol/L的稀硫酸100mL。
①所需仪器除烧杯、玻璃棒外还需 __________、__________、__________。
②所取浓硫酸的体积为____________mL。
③下列操作引起所配溶液浓度偏高的是
| A.用量筒取浓硫酸时俯视 |
| B.将浓硫酸倒出后,洗涤量筒,并将洗涤液倒入烧杯中 |
| C.在烧杯中稀释浓硫酸后,立即转移 |
| D.定容时仰视 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
实验室用NaOH固体配制250mL 1.25mol/L的NaOH溶液,填空并请回答下列问题:
(1)配制250mL 1.25mol/L的NaOH溶液, 应称取NaOH的质量 g;
(2)容量瓶上标有 ;且使用前第一步操作: ;
(3)溶液注入容量瓶前需冷却到室温,这是因为_____________________________;
(4)定容时的操作 ;
(5)下列配制的溶液浓度偏低的是 ;
| A.称量NaOH时,砝码错放在左盘 |
| B.向容量瓶中转移溶液时不慎有液滴洒在容量瓶外面 |
| C.定容时俯视刻度线 |
| D.配制前,容量瓶中有少量蒸馏水 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
(8分)实验室欲用NaOH固体配制1.0 mol/L的NaOH溶液240 mL。
(1)配制溶液时,一般可以分为以下几个步骤:
①称量②计算③溶解④摇匀⑤移液⑥洗涤⑦定容⑧冷却⑨摇动
其正确的操作顺序为____________________(填序号)。本实验必须用到的仪器有托盘
天平、药匙、玻璃棒、烧杯、_______、 。
(2)某同学欲称量NaOH的质量,先用托盘天平称量烧杯的质量,托盘天平平衡后的状
态如图所示。烧杯的实际质量为________g,要完成本实验该同学应称量________g NaOH。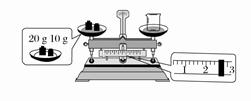
(3)使用容量瓶前必须进行的一步操作是 。
(4)配制过程中,下列操作会引起所配溶液浓度偏高的是
| A.转移溶液时,有少量溶液洒到容量瓶外面 |
| B.定容时俯视刻度线 |
| C.未冷却至室温就将溶液移入容量瓶中并定容 |
| D.定容后塞上瓶塞反复摇匀,静置后,液面低于刻度线,再加蒸馏水至刻度线 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com