
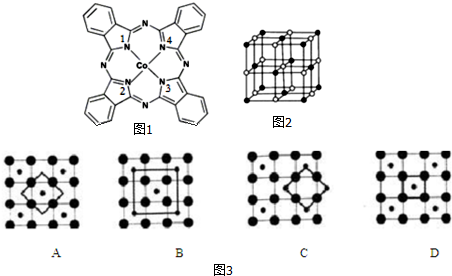
���� ��1��CoΪ27��Ԫ�أ�ԭ�Ӻ��������Ϊ27�������������ԭ����д��������Ų�ʽ��
��2����̪ݼ�������ַǽ���ԭ��ΪC��N��H��ͬ����������ҵ縺�����ǽ�����Խǿ�縺��Խ������Cԭ�Ӿ��γ�3���Ҽ���û�й¶Ե��ӣ��ӻ������ĿΪ3��
�ں��й¶Ե��ӵ�Nԭ����Coͨ����λ����ϣ��γ���λ�����γ�4�Թ��õ��Ӷԣ��γ�3�Թ��õ��ӶԵ�Nԭ���γ���ͨ�Ĺ��ۼ���
��3��ͨ����ɫ�ı仯���Ա����轺����ʪ�̶ȣ�
��4��[Co��CN��6]4-�����Ӿ���ǿ��ԭ�ԣ��ڼ���ʱ����ˮ��Ӧ���ɵ���ɫ[Co��CN��6]3-��ֻ����ˮ����Ԫ�ر���ԭΪ���������ݵ���غ����������������ɣ�
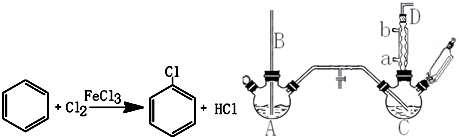
��5���������ᄃ���ṹ��֪������Co��Oԭ����Ŀ֮��Ϊ1��1�������ɫ��ΪCoԭ�ӣ��Զ���Coԭ��Ϊ�о�������֮�Ⱦ������������ԭ��λ�����ģ�ÿ������Ϊ8���������ã�ÿ������Ϊ2���������ã�
CoO2���ظ��ṹ��Ԫʾ��ͼ��Co��Oԭ����Ŀ֮��ӦΪ1��2����Ͼ�̯�������жϣ�
��� �⣺��1��CoΪ27��Ԫ�أ�ԭ�Ӻ��������Ϊ27�������������ԭ�������������Ų�ʽΪ��1s22s22p63s23p63d74s2��
�ʴ�Ϊ��1s22s22p63s23p63d74s2��
��2����̪ݼ�������ַǽ���ԭ��ΪC��N��H��ͬ����������ҵ縺�����ǽ�����Խǿ�縺��Խ�ʵ縺��N��C��H��������Cԭ�Ӿ��γ�3���Ҽ���û�й¶Ե��ӣ��ӻ������ĿΪ3��̼ԭ�ӵ��ӻ��������Ϊ sp2��
�ʴ�Ϊ��N��C��H��sp2��
�ں��й¶Ե��ӵ�Nԭ����Coͨ����λ����ϣ��γ���λ�����γ�4�Թ��õ��Ӷԣ��γ�3�Թ��õ��ӶԵ�Nԭ���γ���ͨ�Ĺ��ۼ���1�š�3��Nԭ���γ�3�Թ��õ��Ӷ�Ϊ��ͨ���ۼ���2�š�4��Nԭ���γ�4�Թ��õ��Ӷԣ���Coͨ����λ����ϣ�
�ʴ�Ϊ��2��4��
��3�����Ź轺����ʪ���ٴκ�ɣ����Ȼ����ڽᾧˮ�������ˮ�μ�ת����ͨ����ɫ�ı仯���Ա����轺����ʪ�̶ȣ�
�ʴ�Ϊ�����Ź轺����ʪ���ٴκ�ɣ����Ȼ����ڽᾧˮ�������ˮ�μ�ת����ͨ����ɫ�ı仯���Ա����轺����ʪ�̶ȣ�
��4��[Co��CN��6]4-�����Ӿ���ǿ��ԭ�ԣ��ڼ���ʱ����ˮ��Ӧ���ɵ���ɫ[Co��CN��6]3-��ֻ����ˮ����Ԫ�ر���ԭΪ���������ݵ���غ����������������ɣ��÷�Ӧ���ӷ���ʽΪ��2[Co��CN��6]4-+2H2O=2[Co��CN��6]3-+H2��+2OH -��
�ʴ�Ϊ��2[Co��CN��6]4-+2H2O=2[Co��CN��6]3-+H2��+2OH -��
��5���������ᄃ���ṹ��֪������Co��Oԭ����Ŀ֮��Ϊ1��1�������ɫ��ΪCoԭ�ӣ��Զ���Coԭ��Ϊ�о�������֮�Ⱦ������������ԭ��λ�����ģ�ÿ������Ϊ8���������ã�ÿ������Ϊ2���������ã��ڸþ�������һ����ԭ�ӵȾ������������ԭ����ĿΪ$\frac{3��8}{2}$=12��
CoO2���ظ��ṹ��Ԫʾ��ͼ��Co��Oԭ����Ŀ֮��ӦΪ1��2����ͼ���֪��
A��Co��Oԭ����Ŀ֮��Ϊ1��4��$\frac{1}{2}$=1��2�����ϣ�
B��Co��Oԭ����Ŀ֮��Ϊ��1+4��$\frac{1}{4}$����4=1��2�����ϣ�
C��Co��Oԭ����Ŀ֮��Ϊ4��$\frac{1}{4}$��4��$\frac{1}{2}$=1��2�����ϣ�
D��Co��Oԭ����Ŀ֮��Ϊ1��4��$\frac{1}{4}$=1��1�������ϣ�
�ʴ�Ϊ��12��D��
���� �����Ƕ����ʽṹ�����ʵĿ��飬�漰��������Ų���������������ȣ����ؿ���ѧ����֪ʶ��������Ǩ��Ӧ�ã�ע�����þ�̯�����о������㣬������λ���γ�������


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ý����ƿɼ����Ҵ������� | |
| B�� | �����Ƶ�������Һ�ɼ�����������ͱ�ȩ | |
| C�� | ��ˮ�ɼ��𱽺��屽 | |
| D�� | �����Ը��������Һ�ɼ������3-��ϩ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ��Ŀ | ���ȱ� | β�� | ��ȷ������ | ��ʧ���� |
| ����ʧ����kg/t�� | 13 | 24.9 | 51.3 | 89.2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��
�� ����������ʽ�ܼӿ췴Ӧ���ʵ�ԭ���ǵ������������˫�����ṹ�����ı䣮
����������ʽ�ܼӿ췴Ӧ���ʵ�ԭ���ǵ������������˫�����ṹ�����ı䣮| X�������� | N-H���� | N-N���� | H-N-H���� |
| ���� | 101.9pm | 339.0pm | 107�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 6 | B�� | 7 | C�� | 8 | D�� | 9 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | NaOH | B�� | Ca��OH��2 | C�� | Mg��OH��2 | D�� | Al��OH��3 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com