
| 稀NaOH溶液 |
| H2O |
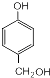 ,可推知X为
,可推知X为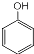 ,根据W的分子式与
,根据W的分子式与 比较,可知
比较,可知 发生氧化反应得W为
发生氧化反应得W为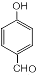 ,
, 与乙醛发生信息Ⅲ的反应生成
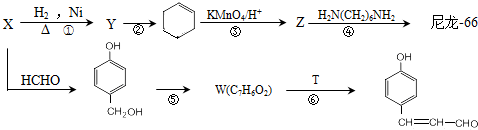
与乙醛发生信息Ⅲ的反应生成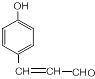 ,所以T为CH3CHO,X与氢气发生加成反应得Y为
,所以T为CH3CHO,X与氢气发生加成反应得Y为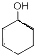 ,Y发生消去反应得环已稀,环已稀被氧化得Z,Z的化学式为C6H10O4,所以Z为HOOHCH2CH2CH2CH2COOH,Z与
,Y发生消去反应得环已稀,环已稀被氧化得Z,Z的化学式为C6H10O4,所以Z为HOOHCH2CH2CH2CH2COOH,Z与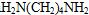 发生缩聚反应生成为尼龙-66为
发生缩聚反应生成为尼龙-66为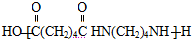 ,据此答题;
,据此答题; ,可推知X为
,可推知X为 ,根据W的分子式与
,根据W的分子式与 比较,可知
比较,可知 发生氧化反应得W为
发生氧化反应得W为 ,
, 与乙醛发生信息Ⅲ的反应生成
与乙醛发生信息Ⅲ的反应生成 ,所以T为CH3CHO,X与氢气发生加成反应得Y为
,所以T为CH3CHO,X与氢气发生加成反应得Y为 ,Y发生消去反应得环已稀,环已稀被氧化得Z,Z的化学式为C6H10O4,所以Z为HOOHCH2CH2CH2CH2COOH,Z与
,Y发生消去反应得环已稀,环已稀被氧化得Z,Z的化学式为C6H10O4,所以Z为HOOHCH2CH2CH2CH2COOH,Z与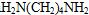 发生缩聚反应生成为尼龙-66为
发生缩聚反应生成为尼龙-66为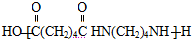 ,
, ,X的化学名称为苯酚,W的结构简式为
,X的化学名称为苯酚,W的结构简式为 ,T为CH3CHO,T的分子式为C2H4O,
,T为CH3CHO,T的分子式为C2H4O, ;C2H4O;
;C2H4O;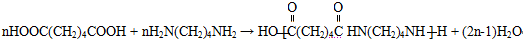 ,反应⑤的类型为氧化反应,
,反应⑤的类型为氧化反应,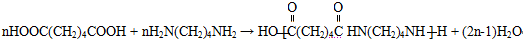 ;氧化反应;
;氧化反应; 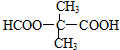 ,
,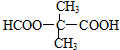 ;
;


 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源: 题型:
| A、导致易拉罐变瘪的离子反应是:CO2+OH-=HCO3- |
| B、导致易拉罐又鼓起来的反应是:Al3++3HCO3-=Al(OH)3+3CO2 |
| C、若将CO2换为NH3,浓NaOH溶液换为水,易拉罐也会出现先瘪后鼓的现象 |
| D、上述过程中与NaOH溶液反应的物质有三种,且反应结束后的溶液显碱性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2 | B、3 | C、4 | D、5 |
查看答案和解析>>
科目:高中化学 来源: 题型:
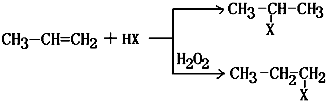 (X)为卤素原子
(X)为卤素原子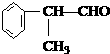 的物质,该物质是一种香料.
的物质,该物质是一种香料.
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素编号 | 元素性质或原子结构 |
| T | 单质能与水剧烈反应,所得溶液呈弱酸性 |
| X | L层p电子数比s电子数多2个 |
| Y | 第3周期元素的简单离子中半径最小 |
| Z | L层有三个未成对电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
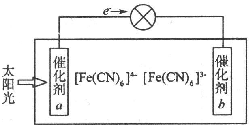 铁、铜等金属及其化合物在日常生活中应用广泛,回答下列问题.
铁、铜等金属及其化合物在日常生活中应用广泛,回答下列问题.
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
45 26 |
45 26 |
| A、它是一种新元素 | ||||
B、
| ||||
| C、它是一种新核素 | ||||
D、这种铁原子发生衰变放出两个质子后变成
|
查看答案和解析>>
科目:高中化学 来源: 题型:
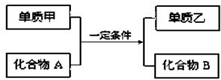 置换反应的通式可表示为如图:单质甲、乙和化合物A、B为中学常见物质,请回答下列问题:
置换反应的通式可表示为如图:单质甲、乙和化合物A、B为中学常见物质,请回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com