
| A. | 向FeCl3溶液中滴加HI溶液:Fe3++2I-═Fe2++I2 | |
| B. | 用铜电极电解氯化钠溶液:2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$Cl2↑+H2↑+2OH- | |
| C. | 向Al2(SO4)3溶液中加入过量氨水:Al3++3NH3•H2O═Al(OH)3↓+3NH4+ | |
| D. | 向Na2SiO3溶液中滴加稀盐酸:Na2SiO3+2H+═H2SiO3↓+2 Na+ |
分析 A.方程式左右电荷不守恒;
B.用铜作阳极电解氯化钠溶液时,阳极上铜失电子生成铜离子;
C.向Al2(SO4)3溶液中加入过量氨水生成氢氧化铝和硫酸铵,氢氧化铝不溶于弱碱;
D.硅酸钠与氯化氢反应生成硅酸沉淀和氯化钠,硅酸钠为易溶于水易电离的盐,应拆写.
解答 解:A.氯化铁具有氧化性,碘化氢中-1价的碘离子具有还原性,两者发生氧化还原反应生成碘单质和亚铁离子,反应为:2Fe3++2I-═2Fe2++I2,故A错误;
B.用铜作阳极电解氯化钠溶液时,阳极上铜失电子而不是电解质溶液中氯离子失电子,所以得不到氯气,故B错误;
C.Al2(SO4)3溶液中加入过量氨水反应生成氢氧化铝和硫酸铵,离子方程式Al3++3NH3•H2O═Al(OH)3↓+3NH4+,故C正确;
D.向Na2SiO3溶液中滴加稀盐酸:SiO32-+2H+═H2SiO3↓,故D错误;
故选C.
点评 本题考查了离子方程式的书写,明确反应实质是解题关键,注意氢氧化铝不溶于弱碱为易错选项,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 我国首艘航母“辽宁舰”上用于载机降落的拦阻索是特种钢缆,属于金属材料 | |
| B. | 研制高性能的耐磨轮胎,可减少PM2.5等颗粒物的产生 | |
| C. | 采用纳米TiO2光触媒技术,将装修材料中释放的HCHO转化为无害物质 | |
| D. | 高纯度的硅单质广泛用于光导纤维,光导纤维遇强碱会造成“短路” |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 石灰石溶于稀盐酸:CaCO3+2H+═Ca2++CO2↑+H2O | |
| B. | 硫酸铜溶液与氢氧化钡溶液反应:Ba2++SO42-═BaSO4↓ | |
| C. | 氧化镁与稀硫酸:MgO+2H+═Mg2++H2O | |
| D. | 常温下,将铜片插入硝酸银溶液中:Cu+Ag+═Cu2++Ag |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe2+、Na+、SO42-、NO3- | B. | Al3+、K+、Cl-、HCO3- | ||
| C. | Na+、Fe3+、NO3-、CO32- | D. | Mg2+、NH4+、SO42-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在稀溶液中,H+(aq)+OH-(aq)=H2O(l);△H=-57.3kJ/mol,若将含0.5molH2SO4的浓硫酸与含1molNaOH的溶液混合,放出的热等于57.3kJ | |
| B. | 在一密闭容器中发生反应2SO2+O2?2SO3,增大压强,平衡正向移动,K增大 | |
| C. | 2C(s)+O2(g)═2CO(g)△H=-221 kJ•mol-1,则C的燃烧热△H=-110.5 kJ•mol-1 | |
| D. | 向稀硫酸中加入少量硫酸铜可提高锌与稀硫酸反应生成氢气的速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
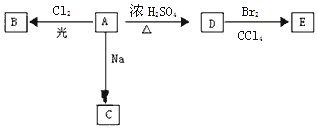
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在水溶液中可以显酸性的物质是酸 | |
| B. | 电离时产生的阳离子中有H+的化合物是酸 | |
| C. | 电离时产生的阴离子全部是OH-的化合物是碱 | |
| D. | 盐只能电离出金属阳离子和酸根离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷的标准燃烧热为△H=-890.3kJ•mol-1,则甲烷燃烧的热化学方程式可表示为CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890.3 kJ•mol-1 | |
| B. | 500℃、30MPa下,将0.5mol N2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为 N2(g)+3H2(g)?2NH3(g)△H=-38.6kJ•mol-1 | |
| C. | 常温常压下,酸与碱反应生成1mol水时所放出的热量一定为57.3KJ | |
| D. | 放热反应的△H一定比吸热反应小 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com