
| A. | 镀锌铁片比镀锡铁片更耐腐蚀 | |
| B. | 远洋海轮的尾部装上一定数量的锌板 | |
| C. | 用锌与硫酸制氢气时,往硫酸中滴少量硫酸铜 | |
| D. | 常温条件下,在空气中铝不易被腐蚀 |
分析 A.作原电池负极的金属加速被腐蚀,作原电池正极的金属被保护;
B.作原电池正极的金属被保护;
C.构成原电池时加速负极被腐蚀;
D.常温下,铝极易和氧气反应生成氧化铝,致密的氧化铝不易被腐蚀.
解答 解:A.镀锌铁片中Fe作正极被保护,镀锡铁片中Fe作负极加速被腐蚀,所以镀锌铁片比镀锡铁片更耐腐蚀,能用电化学原理解释,故A不选;
B.Zn、Fe和海水构成原电池,Fe作正极被保护,所以远洋海轮的尾部装上一定数量的锌板,可以用电化学原理解释,故B不选;
C.Zn和铜离子发生置换反应生成Cu,Cu、Zn和稀硫酸构成原电池而加速Zn被腐蚀,则加快化学反应速率,可以用电化学原理解释,故C不选;
D.常温下,铝极易和氧气反应生成氧化铝,致密的氧化铝不易被腐蚀,不能构成原电池,则不能用电化学原理解释,故D选;
故选D.
点评 本题考查电化学原理,为高频考点,侧重考查学生分析判断能力,明确原电池原理是解本题关键,知道原电池构成条件,题目难度不大.


 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案科目:高中化学 来源: 题型:选择题
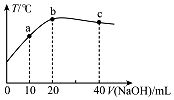 在一隔热系统中,向20.00mL 0.01000mol•L-1的醋酸溶液中逐滴加入0.01000mol.L-1的NaOH溶液,测得混合溶液的温度变化如图.下列相关说法正确的是( )
在一隔热系统中,向20.00mL 0.01000mol•L-1的醋酸溶液中逐滴加入0.01000mol.L-1的NaOH溶液,测得混合溶液的温度变化如图.下列相关说法正确的是( )| A. | 若a点溶液呈酸性,则a点有:c(CH3COO-)>c(Na+)>c(CH3COOH) | |
| B. | 从b到c:$\frac{c(C{H}_{3}COOH)}{c(C{H}_{3}CO{O}^{-})}$逐渐增大 | |
| C. | 水的电离程度:b点<c点 | |
| D. | b点有0.01000mol•L-1+c(H+)=c(Na+)-c(CH3COOH)+c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
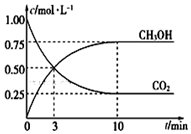 根据现代工业技术可以用H2和CO反应来生产燃料甲醇,其反应方程式如下:CO2 (g)+3H2(g)?H2O(l)+CH3OH(g)△H=-49.00kJ•mol-1
根据现代工业技术可以用H2和CO反应来生产燃料甲醇,其反应方程式如下:CO2 (g)+3H2(g)?H2O(l)+CH3OH(g)△H=-49.00kJ•mol-1查看答案和解析>>
科目:高中化学 来源: 题型:选择题
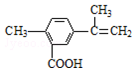
| A. | 在一定条件下,能发生取代、氧化、酯化反应 | |
| B. | 1 mol该物质最多可与2 molNa反应 | |
| C. | 1 mol该物质最多可与4 mol H2发生加成反应 | |
| D. | 1 mol该物质完全氧化最多可消耗13 mol氧气 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 浓度均为0.2mol•L-1的NH4Cl溶液与NaOH溶液混合,c(NH4+)>c(Cl-)>c(Na+)>c(OH-)>c(H+) | |
| B. | 仅含有Na+、H+、OH-、CH3COO-四种离子的某溶液中可能存c(Na+)>c(OH-)>c(CH3COO-)>c(H+) | |
| C. | 常温下,pH=2的醋酸与pH=12的氢氧化钠等体积混合后,混合液中c(Na+)>c(CH3COO-)>c(OH-)>c(H+) | |
| D. | 将pH=8.5的氨水加水稀释后,溶液中所有离子的浓度均降低 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分别同时滴入等浓度的盐酸,放出气体NaHCO3比Na2CO3快 | |
| B. | 热稳定性Na2CO3<NaHCO3 | |
| C. | 常温时水溶性Na2CO3<NaHCO3 | |
| D. | 相对分子质量Na2CO3<NaHCO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com