
分析 先根据n=$\frac{V}{{V}_{m}}$求氯化氢的物质的量,再根据溶液的质量、密度求出溶液的体积,根据物质的量浓度公式c=$\frac{n}{V}$计算该盐酸的物质的量的浓度.
解答 解:标况下aL氯化氢的物质的量为:n=$\frac{aL}{22.4L/mol}$=$\frac{a}{22.4}$mol,氯化氢的质量为:m=n×M=$\frac{a}{22.4}$mol×36.5g/mol=$\frac{36.5a}{22.4}$g,
溶液的质量为:1000g+$\frac{36.5a}{22.4}$g,则该体积为:V=$\frac{m}{ρ}$=$\frac{1000g+\frac{36.5a}{22.4}g}{1000bg/L}$=$\frac{22400+36.5a}{22.4b}$×10-3L,
则该盐酸的物质的量浓度为:c=$\frac{\frac{a}{22.4}mol}{\frac{22400+36.5a}{22.4b}×1{0}^{-3}L}$=$\frac{1000ab}{22400+36.5a}$mol/L,
答:该盐酸的物质的量的浓度为$\frac{1000ab}{22400+36.5a}$mol/L.
点评 本题考查了物质的量浓度的计算,题目难度中等,明确物质的量浓度的概念及表达式为解答关键,试题培养了学生的分析能力及化学计算能力.


科目:高中化学 来源: 题型:选择题
| A. | 在pH=l的溶液中:SO32-、NH4+、ClO-、Cl- | |
| B. | 有SO42-存在的溶液中:Na+、Mg2+、Ba2+、I- | |
| C. | 有NO3-存在的强酸性溶液中:NH4+、Ba2+、Fe2+、Br- | |
| D. | 在c(H+)=1.0×10-13mol•L-1的溶液中:Na+、SO42-、AlO2-、SO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe3+、NH4+、SCN-、C1- | B. | Na+、Br-、NH4+、SO42- | ||
| C. | Na+、HCO3-、K+、CO32- | D. | Fe2+、NH4+、C1-、OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
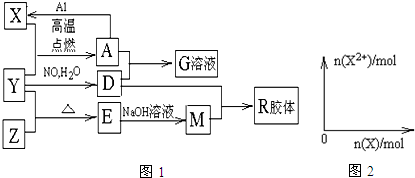
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
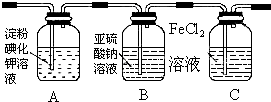
| 实验步骤 | 预期现象和结论 |
| 步骤1:取适量洗气瓶B中溶液于试管A中,滴加过量2 mol/LHCl和1 mol/LBaCl2溶液,振荡. | 若产生的白色沉淀,则洗气瓶B溶液中存在SO42-. |
| 步骤2:另取适量洗气瓶B中溶液于试管B中,滴加过量l mol/LBa(NO3)2溶液,振荡,静置. | 产生白色沉淀. |
| 步骤3:取步骤2后试管B中的上层清液于试管C中,滴加0.1mol/LAgNO3溶液和过量的2mol/LHNO3,振荡. | 若产生白色沉淀,则洗气瓶B溶液中存在Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
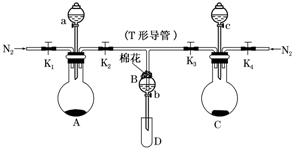 某实验小组用如图所示装置进行实验以探究Fe3+、Cl2和SO2的氧化性强弱(夹持仪器已略).
某实验小组用如图所示装置进行实验以探究Fe3+、Cl2和SO2的氧化性强弱(夹持仪器已略).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常见铅蓄电池放电时,负极质量减轻,正极质量增加 | |
| B. | 电解法精炼铜时,以粗铜作阴极,纯铜作阳极 | |
| C. | 常温下,pH=5的盐酸稀释1000倍后,溶液的pH=8 | |
| D. | 水的离子积随温度升高而增大,说明水的电离是吸热反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com