
分析 Ⅰ.若Fe2O3中含有FeO,利用稀酸(非氧化性)溶解后生成的亚铁离子,则具有还原性,而给出的试剂中KMnO4溶液具有强氧化性,可利用KMnO4溶液褪色来证明;根据检验方法写出实验操作时的步骤、实验现象和结论;
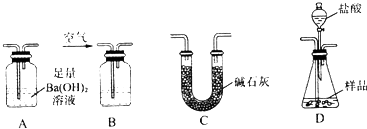
Ⅱ.(1)盛放盐酸的仪器为分液漏斗;先分析实验方案,利用装置B除去空气中的二氧化碳,然后用空气将装置D产生的二氧化碳完全赶到装置A中,为了避免空气中水和二氧化碳干扰,装置A需要连接吸收二氧化碳和水的装置,据此对装置进行排序;
(2)根据通入空气还可以将碳酸钙与盐酸反应生成的二氧化碳驱赶到装置B中分析;
(3)空气中含有二氧化碳,会影响实验测定,需要用氢氧化钠溶液吸收;
(4)由于反应生成的二氧化碳中含有杂质氯化氢和水,导致测定的装置A的质量差增大,测定碳酸钙质量偏大,氧化铁的质量分数偏低.
解答 解:Ⅰ.若Fe2O3中含有FeO,利用稀酸(非氧化性)溶解后生成的亚铁离子,则具有还原性,而给出的试剂中KMnO4溶液具有强氧化性,可使KMnO4溶液褪色,
则选择试剂为稀硫酸、KMnO4溶液;实验操作时的步骤、实验现象和结论为:取少量样品溶于试管中,配成溶液后,再滴入几滴稀硫酸和几滴KMnO4溶液,只要溶液不褪色或不变浅,即说明样品中无FeO,
故答案为:取少量样品溶于试管中,配成溶液后,再滴入几滴稀硫酸和几滴KMnO4溶液,只要溶液不褪色或不变浅,即说明样品中无FeO;
Ⅱ.(1)根据图示可知,盛放盐酸的装置为分液漏斗;测定样品中Fe2O3的质量分数,先根据碳酸钙产生的二氧化碳的质量计算出碳酸钙的质量,再根据样品质量计算出氧化铁的质量分数,仪器连接顺序为:先将空气通入盛有氢氧化钠溶液的装置B,以便除去空气中的二氧化碳,然后利用空气将装置D中产生的二氧化碳驱赶到装置A,利用二氧化碳与氢氧化钡生成的碳酸钡沉淀的质量计算出碳酸钙的质量,由于空气中的二氧化碳、水蒸气影响测定结果,需要在装置A后连接一个吸收二氧化碳、水蒸气的装置C,所以装置连接顺序为:BDAC,
故答案为:分液漏斗;B;D;A;C;
(2)实验过程中需要持续通入空气,其作用除可以起到“搅拌”A、D中反应物达到充分反应外,还可以使反应生成的二氧化碳尽可能彻底的赶入装置A中,使反应生成的二氧化碳能够被氢氧化钡溶液完全吸收,
故答案为:将反应产生的CO2气体尽可能彻底的赶入装置A中,使之完全被Ba(OH)2溶液吸收;
(3)空气中含有二氧化碳,会影响实验测定,而装置B中应该盛放氢氧化钠溶液,从而吸收空气中的二氧化碳,避免空气中的二氧化碳影响测定结果,故d正确,
故答案为:d;
(4)由于装置D生成的二氧化碳中混有氯化氢和水,导致装置A在吸收反应产生的气体前后的质量差偏大,测定的二氧化碳的质量偏大,碳酸钙的质量会偏大,样品中氧化铁的质量偏小,氧化铁的质量分数会偏低,
故答案为:偏低.
点评 本题考查了测定物质的组成的方法,题目难度中等,明确亚铁离子具有还原性是检验氧化亚铁存在的关键,注意根据实验现象和结论的关系来解答,本题在注重对学生基础知识训练和检验的同时,侧重对学生实验答题能力的培养和方法与技巧的指导和训练,有利于提高学生的实验设计能力和应试能力.


科目:高中化学 来源: 题型:选择题
| A. | 天然气的主要成分是甲烷 | |
| B. | 煤是由有机物和无机物组成的复杂的混合物 | |
| C. | 含C18以上烷烃的重油经裂化可以得到汽油 | |
| D. | 煤中含有苯和甲苯,可以用先干馏后分馏的方法把它们分离出来 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 聚苯乙烯单体的分子式为C8H8 | |
| B. | 聚苯乙烯属于纯净物 | |
| C. | 聚苯乙烯能与溴水发生加成反应 | |
| D. | 聚苯乙烯是可降解塑料,不会造成白色污染 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol苯分子中含有C=C双键数目为3NA | |
| B. | 标准状况下,11.2 L CCl4中含有的共价键数目为2NA | |
| C. | 1 mol乙烯和乙醇的混合物完全燃烧时消耗O2的分子数为3NA | |
| D. | 常温常压下,17 g 羟基含有的电子总数为10NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.002 0 | B. | 0.011 | C. | 0.11 | D. | 0.22 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ba(OH)2•8H2O与NH4Cl反应 | |
| B. | 葡萄糖在人体内氧化分解 | |
| C. | 二氧化碳与赤热的碳反应生成一氧化碳 | |
| D. | 锌粒与稀H2SO4反应制取H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
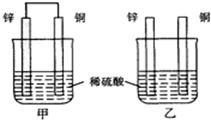
| A. | 两烧杯中溶液的氢离子浓度均减小 | B. | 甲中铜片是正极,乙中铜片是负极 | ||
| C. | 两烧杯中铜片表面均有气泡产生 | D. | 甲、乙溶液均变蓝色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 不用碳酸钡作为内服造影剂,是因为Ksp(BaCO3)>Ksp(BaSO4) | |
| B. | 抢救钡离子中毒患者时,若没有硫酸钠,可以用碳酸钠溶液代替 | |
| C. | 若误饮c(Ba2+)=1.0×10-5 mol•L-1的溶液时,会引起钡离子中毒 | |
| D. | 可以用0.36 mol•L-1的Na2SO4溶液给钡离子中毒患者洗胃 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 作消毒剂的医用酒精是无水酒精 | |
| B. | 通常状况下,不能与金属钠反应 | |
| C. | 在加热和有银存在下,可与氧气反应生成乙醛 | |
| D. | 在水溶液中能够电离产生H+离子,呈现弱酸性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com