
| A、气体密度不再发生变化 |
| B、A、B的物质的量浓度之比等于1:2 |
| C、容器内总压强不再改变 |
| D、单位时间内消耗n mol A,同时消耗2n mol B |


 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案 期末好成绩系列答案
期末好成绩系列答案科目:高中化学 来源: 题型:
| A、H2O>H2Te>H2Se>H2S |
| B、He>Ne>Ar>Kr |
| C、I2>Br2>Cl2>F2 |
| D、GeH4>SiH4>CH4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、5、2、2 |
| B、7、3、2 |
| C、6、2、4 |
| D、5、3、4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1:4 | B、3:4 |
| C、4:1 | D、4:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①② | B、②③ | C、①④ | D、③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
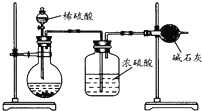 为了测定氢氧化钠和碳酸钠固体混合物中碳酸钠的质量分数,甲、乙两位同学分别设计了如下的实验方案:
为了测定氢氧化钠和碳酸钠固体混合物中碳酸钠的质量分数,甲、乙两位同学分别设计了如下的实验方案:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在自然界中存在的单质,一定具备化学性质稳定、不与其它物质发生反应这一特征 |
| B、100多年前,英国曾耗巨资改建高炉,试图延长CO和Fe2O3的接触时间,以减少CO的排放,这违背了化学反应都有一定限度这一基本原理 |
| C、在溶液中,有色物质参与的反应,可以用分光光度计来测定其化学反应速率 |
| D、虽然碳酸钙分解需要吸收大量的热,但在高温条件下也能自发进行 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com