


 小学教材完全解读系列答案
小学教材完全解读系列答案科目:高中化学 来源: 题型:
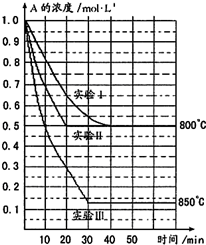 在一恒容密闭容器中发生某化学反应:2A(g)?B(g)+C(g)(A气体有颜色),在三种不同条件下进行,其中实验Ⅰ、Ⅱ都在800℃,实验Ⅲ在850℃,B、C的起始浓度都为0,反应物A的浓度(mol?L-1)随时间(min)的变化如图所示:试回答下列问题:
在一恒容密闭容器中发生某化学反应:2A(g)?B(g)+C(g)(A气体有颜色),在三种不同条件下进行,其中实验Ⅰ、Ⅱ都在800℃,实验Ⅲ在850℃,B、C的起始浓度都为0,反应物A的浓度(mol?L-1)随时间(min)的变化如图所示:试回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 (1)在原电池中,通常较活泼的金属做
(1)在原电池中,通常较活泼的金属做查看答案和解析>>
科目:高中化学 来源: 题型:
| A、油的熔点低,脂肪的熔点高 |
| B、油含不饱和烃基的相对量比脂肪少 |
| C、油和脂肪都不易溶于水,易溶于汽油、酒精、苯等有机溶剂 |
| D、油经过氢化可以转化为脂肪,通常又叫做硬化油 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、淀粉、纤维素、油脂都属于高分子化合物 |
| B、油脂水解得到的醇是丙三醇 |
| C、酶只有在强酸性或强碱性条件下才能发挥作用 |
| D、可溶性铜盐可以使蛋白质产生盐析 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、为了加快过滤速度,可用玻璃棒搅拌过滤器中的液体 |
| B、为了防止蒸馏时温度过高,可将温度计插入液面以下 |
| C、为了使制取氢气的速率加快,可向稀硫酸中加入少量硫酸铜溶液 |
| D、为了使配制的FeCl3溶液不产生浑浊,可加入盐酸和铁片 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、S2- NO3- NH4+ K+ |
| B、OH- Na+ Cl- K+ |
| C、NO3- Fe3+ Cl- SO42- |
| D、SO32- H+ K+ NO3- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com