
【题目】用如图所示的装置进行电解。通电一段时间后,发现湿润的淀粉-KI试纸的C端变为蓝色。
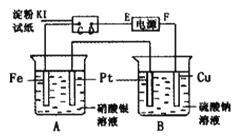
(1)E为电源的_________极F为电源的_________极
(2)A中发生反应的化学方程式为____________________________________。
(3)在B端观察到的现象是_____________________________________________。
(4)D端的电极反应式为_____________________________________________。
【答案】负 正 4AgNO3+2H2O![]() 4Ag+4HNO3+O2↑ 铜片溶解,石墨电极上有气体生成,溶液中有蓝色沉淀生成 2H++2e-===H2↑
4Ag+4HNO3+O2↑ 铜片溶解,石墨电极上有气体生成,溶液中有蓝色沉淀生成 2H++2e-===H2↑
【解析】
通电一段时间后,发现湿润的淀粉KI试纸的C端变为蓝色,则C端发生2I--2e-=I2,C端为阳极,D为阴极,即E为电源的负极,F为电源的正极,结合离子的放电顺序及发生的电极反应来计算解答。
(1)根据以上分析可知C端为阳极,D为阴极,E为电源的负极,F为电源的正极;
(2)A烧杯中铁电极与电源的负极相连,作阴极,银离子放电,Pt电极是阳极,氢氧根离子放电,因此发生电解硝酸银溶液的反应,反应为4AgNO3+2H2O![]() 4Ag+4HNO3+O2↑;
4Ag+4HNO3+O2↑;
(3)B烧杯中铜电极是阳极,发生反应:Cu-2e-=Cu2+,阴极氢离子放电,电极反应式为2H++2e-=H2↑,水的电离平衡被破坏,产生氢氧根,氢氧根结合铜离子生成氢氧化铜沉淀,所以在B中观察到的现象是铜片溶解,石墨电极上有气体生成,溶液中有蓝色沉淀生成;
(4)因D电极为阴极,氢离子放电,电极反应为2H++2e-=H2↑。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】如图所涉及的物质均为中学化学中的常见物质,其中D为黄绿色的气体,E为Fe单质,它们存在如下转化关系,反应中生成的水及次要产物均已略去.
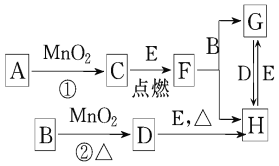
(1)写出有关物质的名称:B__________,F______________
(2)写出F与金属铝在高温下的反应化学方程式____________________________
(3)若反应①是在加热条件下进行的,则A是____________ (填化学式);
(4)指出MnO2在相关反应中的作用:反应②中是________剂.
(5)写出B与MnO2共热获得D的化学方程式: __________________________.
(6)实验室检验H中的阳离子的方法是______________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2A+B![]() 3C+4D反应中,表示该反应速率最快的是
3C+4D反应中,表示该反应速率最快的是
A. v(B)=0.3 mol·L-1· s-1B. v(A)=0.5mol·L-1· s-1
C. v(C)=0.8 mol·L-1· s-1D. v(D)=30 mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A(C2H4)是基本的有机化工原料。用A和常见的有机物可合成一种醚类香料和一种缩醛类香料。具体合成路线如图所示 ( 部分反应条件略去 ):
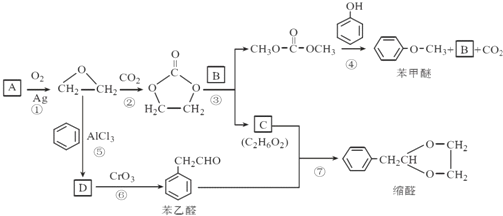
已知:①![]()
②D为单取代芳香族化合物且能与金属钠反应;每个D分子中只含有1个氧原子,D中氧元素的质量分数约为13.1%.
回答下列问题:
(1)A的名称是 ___ ,图中缩醛的分子式是 ___.
(2)B的结构简式为 ___.
(3)⑤的化学方程式为 ___.
(4)⑥的反应类型是 ___.
(5)请写出核磁共振氢谱有 4 组峰 , 峰面积之比为 3:2:2:1, 并含有苯环和![]() 结构的苯乙醛的所有同分异构体的结构简式: ___.
结构的苯乙醛的所有同分异构体的结构简式: ___.
(6)参照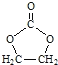 的合成路线,设计一条由2氯丙烷和必要的无机试剂制备
的合成路线,设计一条由2氯丙烷和必要的无机试剂制备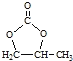 的合成路线(注明必要的反应条件 )___。
的合成路线(注明必要的反应条件 )___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1) 一定温度下,向1 L 0.l mol·L-1 CH3 COOH溶液中加入0.1 molCH3COONa固体,溶液中![]() __________________(填“增大”、“减小”或“不变”)。
__________________(填“增大”、“减小”或“不变”)。
(2)常温下,将VmL、0.1000mol·L-1氢氧化钠溶液逐滴加入到20.00mL、0.1000mol·L-1醋酸溶液中,充分反应。回答下列问题。(忽略溶液体积的变化)
①如果溶液pH=7,此时V的取值___________20.00(填“>”、“<”或“=”),而溶液中 c(Na+)、c(CH3COO-)、c(H+)、c(OH-)的大小关系为_____________________________。
②如果V=40.00,则此时溶液中c(OH-) -c(H+) - c(CH3COOH)= _________mol·L-1。
(3)常温下,向20 ml 0.1mol·L-1 Na2CO3溶液中逐滴加入0.1mol·L-1 HC1溶液40 mL,溶液中含碳元素的各种微粒(CO2因逸出未画出)物质的量分数随溶液pH变化的情况如下图,回答下列问题:

①若将Na2CO3和NaHCO3混合物配成溶液,则此溶液的pH的取值范围是________________;
为测定Na2CO3和NaHCO3混合物中的质量分数,下列方案可行的是_________________
A.取a克混合物充分加热,减重b克
B.取a克混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得b克固体
C.取a克混合物与足量稀硫酸充分反应,逸出气体用碱石灰吸收,增重b克
D.取a克混合物与足量Ba(OH)2溶液充分反应,过滤、洗涤、烘干,得b克固体
②所得溶液中含量最多的三种离子的物质的量浓度的大小关系为_________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成氨反应为:3H2+N2 ![]() 2NH3,其反应速率可以分别用v(H2)、v(N2)、v(NH3)表示,反应达平衡时,下列关系式正确的是 ( )
2NH3,其反应速率可以分别用v(H2)、v(N2)、v(NH3)表示,反应达平衡时,下列关系式正确的是 ( )
A. 3v(H2)正=v(N2)逆 B. v(H2)生成=v(NH3)生成
C. 2v(N2)消耗=v(NH3)消耗 D. 3v(H2)逆=2v(NH3)正
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,向下列溶液中通入相应的气体至溶液pH=7(忽略溶液体积的变化),溶液中部分微粒的物质的量浓度不正确的是 ( )
A. 向0.20 mol/L NH4HCO3中通入CO2: C(NH4+)=C(HCO3-)+2C(CO32-)
B. 向0.15 mol/L NaHSO3中通入NH3: C(Na+)>C(NH4+)>C(SO32-)
C. 向0.30mol/L Na2SO3中通入CO2: C(Na+)=2[C(SO32-)+C(HSO3-)+C(H2SO3)]
D. 向0.10 mol/L CH3COONa中通入HCl:C(Na+)>C(CH3COOH)=C(Cl-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】两种金属粉末的混合物12g,投入足量的稀硫酸中,在标准状况下产生11.2L气体,则这种混合物可能是( )
A. Zn、Al B. Fe、Zn C. Al、Mg D. Mg、Cu
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质中,既能因发生化学反应使溴水褪色,又能使酸性KMnO4溶液褪色的是
①SO2 ②CH3CH2CH=CH2 ③![]() ④ CH3CH3
④ CH3CH3
A. ①②③④B. ③④
C. ①②④D. ①②
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com