
| A. | 用酸性KMnO4溶液能鉴别CH3CH═CHCH2OH和CH3CH2CH2CHO | |
| B. | 乙酸乙酯能水解,可用于制备肥皂 | |
| C. | 根据核磁共振氢谱不能鉴别1-溴丙烷和2-溴丙烷 | |
| D. | 食用花生油和鸡蛋清都能发生水解反应 |
分析 A.碳碳双键、-OH、-CHO均能被高锰酸钾氧化;
B.油脂在碱性条件下水解,为皂化反应;
C.1-溴丙烷和2-溴丙烷分别含H的种类为3、2;
D.食用花生油为油脂,鸡蛋清的成分为蛋白质.
解答 解:A.碳碳双键、-OH、-CHO均能被高锰酸钾氧化,则酸性KMnO4溶液不能鉴别CH3CH═CHCH2OH和CH3CH2CH2CHO,故A错误;
B.油脂在碱性条件下水解,为皂化反应,乙酸乙酯水解不能制备肥皂,故B错误;
C.1-溴丙烷和2-溴丙烷分别含H的种类为3、2,则核磁共振氢谱能鉴别1-溴丙烷和2-溴丙烷,故C错误;
D.食用花生油为油脂,鸡蛋清的成分为蛋白质,均可发生水解反应,故D正确;
故选D.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系、有机反应为解答的关键,侧重分析与应用能力的考查,注意有机物的性质差异,题目难度不大.


 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案 导学教程高中新课标系列答案
导学教程高中新课标系列答案科目:高中化学 来源: 题型:选择题
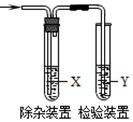 用如图所示装置检验乙烯时不需要除杂的是( )
用如图所示装置检验乙烯时不需要除杂的是( )| 乙烯的制备 | 试剂X | 试剂Y | |
| A | CH3CH2Br与NaOH乙醇溶液共热 | 水 | KMnO4酸性溶液 |
| B | CH3CH2Br与NaOH乙醇溶液共热 | 水 | Br2的CCl4溶液 |
| C | C2H5OH与浓H2SO4加热至170℃ | NaOH溶液 | KMnO4酸性溶液 |
| D | C2H5OH与浓H2SO4加热至170℃ | NaOH溶液 | Br2的CCl4溶液 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
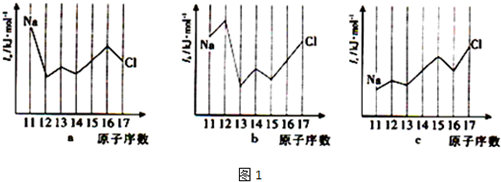
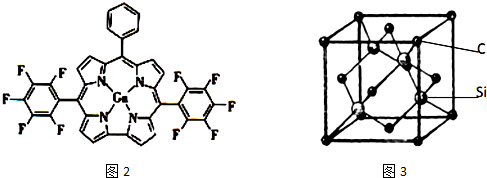
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,砷属于p区元素.
,砷属于p区元素.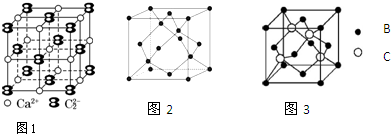
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{48}^{112}$Cd原子的中子数为64 | |
| B. | 聚氯化铝能降污是因为它有强氧化性 | |
| C. | 聚氯化铝是混合物 | |
| D. | 镉的单质有导电性和延展性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com