
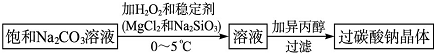
分析 过氧化氢为液体,难以贮存和运输,工业常见过氧化氢转化为过碳酸钠,生成时将反应温度控制在0~5℃,目的是防止在较低温度下2Na2CO3•3H2O2溶解度更小,且过氧化氢和过碳酸钠较稳定,加入稳定剂,发生MgCl2+Na2SiO3=MgSiO3↓+2NaCl,不溶物将过碳酸钠粒子包住,得到稳定的溶液,在溶液中加入异丙醇可以减小过碳酸钠在水的溶解度,使过碳酸钠晶体析出而得到过碳酸钠晶体,
(1)过氧化氢溶液加入二氧化锰的发生分解反应生成水和氧气;
(2)在低温时H2O2与2Na2CO3•3H2O2稳定(不易分解)且2Na2CO3•3H2O2的溶解度小;
(3)根据元素守恒可书写化学方程式;
(4)过碳酸钠在异丙醇中的溶解度较小;
(5)过碳酸钠在铁离子作催化剂、酸性条件及还原剂的条件下都容易失效;
(6)由于2Na2CO3•3H2O2具有Na2CO3和Na2O2的双重性质,可从过氧化氢和碳酸钠的性质的角度选择贮存、运输过碳酸钠晶体中应注意的事项;
(7)酸性高锰酸钾溶液与过氧化氢溶液发生氧化还原反应生成锰离子和氧气,根据电荷守恒和元素守恒书写离子方程式.
解答 解:过氧化氢为液体,难以贮存和运输,工业常见过氧化氢转化为过碳酸钠,生成时将反应温度控制在0~5℃,目的是防止在较低温度下2Na2CO3•3H2O2溶解度更小,且过氧化氢和过碳酸钠较稳定,加入稳定剂,发生MgCl2+Na2SiO3=MgSiO3↓+2NaCl,不溶物将过碳酸钠粒子包住,得到稳定的溶液,在溶液中加入异丙醇可以减小过碳酸钠在水的溶解度,使过碳酸钠晶体析出而得到过碳酸钠晶体,
(1)过氧化氢溶液加入二氧化锰的发生分解反应生成水和氧气,反应的方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,
故答案为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(2)在低温时H2O2与2Na2CO3•3H2O2稳定(不易分解)且2Na2CO3•3H2O2的溶解度小,便于生成过碳酸钠,
故答案为:在低温下H2O2与2Na2CO3•3H2O2稳定(不易分解)且2Na2CO3•3H2O2的溶解度小;
(3)根据上面的分析可知,反应的化学方程式为MgCl2+Na2SiO3=MgSiO3↓+2NaCl,
故答案为:MgCl2+Na2SiO3=MgSiO3↓+2NaCl;
(4)过碳酸钠在异丙醇中的溶解度较小,所以加入异丙醇的作用为降低过碳酸钠的溶解度,有利于晶体析出,
故答案为:降低过碳酸钠的溶解度,有利于晶体析出;
(5)过碳酸钠在铁离子作催化剂、酸性条件及还原剂的条件下都容易失效,a.FeCl3 对过碳酸钠的分解起催化作用; b.Na2S具有还原性,能还原过碳酸钠;c.CH3COOH 具有酸性,过碳酸钠能与酸反应,过碳酸钠较在碳酸氢钠中较稳定,故选 d;
(6)由于2Na2CO3•3H2O2具有Na2CO3和Na2O2的双重性质,所以贮存、运输过碳酸钠晶体中应注意密封防潮、避免高温、避免接触还原性、酸性或二氧化锰、铁盐等物质,
故答案为:密封防潮、避免高温、避免接触还原性、酸性或二氧化锰、铁盐等物质(写出其中两项即可);
(7)酸性高锰酸钾溶液与过氧化氢溶液发生氧化还原反应生成锰离子和氧气,反应的离子方程式为5H2O2+2MnO${\;}_{4}^{-}$+6H+═2Mn2++5O2↑+8H2O,
故答案为:5H2O2+2MnO${\;}_{4}^{-}$+6H+═2Mn2++5O2↑+8H2O.
点评 本题考查物质制备的实验设计,侧重于钠的化合物的考查,注意把握制备原理,结合题给信息解答,答题时注意审题,要具备较强的审题能力和自学能力.


科目:高中化学 来源:2017届河北省高三上期中化学试卷(解析版) 题型:选择题
ClO2是一种广谱型的消毒剂,根据世界环保联盟的要求ClO2将逐渐取代Cl2成为生产自来水的消毒剂。工业上ClO2常用NaClO3和Na2SO3溶液混合并加H2SO4酸化后反应制得,在以上反应中NaClO3和Na2SO3的物质的量之比为
A.1︰1 B. 2︰1 C. 1︰2 D. 2︰3
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 草酸是一种重要的化工原料,常用于有机合成,它属于二元弱酸,易溶于乙醇、水、微溶于乙醚.以甘蔗碎渣(主要成分为纤维素)为原料制取草酸的工艺流程如下:
草酸是一种重要的化工原料,常用于有机合成,它属于二元弱酸,易溶于乙醇、水、微溶于乙醚.以甘蔗碎渣(主要成分为纤维素)为原料制取草酸的工艺流程如下:查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 容器中混合气体的质量不随时间变化 | |
| B. | 容器内三种气体 AB、A2、B2共存 | |
| C. | v正(AB)=2v逆(A2) | |
| D. | 单位时间内消耗n mol A2,同时生成2n mol AB |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②③ | C. | ③④ | D. | ②④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com