
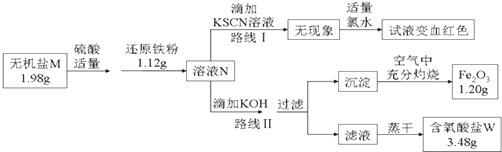
分析 (1)除去混合气体中二氧化碳和水,可以选用碱石灰;
(2)根据化合物中总化合价为0计算出优氯净 Cl2Na(NCO)3中Cl元素的化合价;亚硫酸钠若变质,溶液中会存在硫酸钠,先用过量盐酸除去亚硫酸根离子,然后用氯化钡检验是否含有硫酸根离子,从而判断亚硫酸钠是否变质;
(3)1.2g氧化铁的物质的量为:$\frac{1.2g}{160g/mol}$=0.0075mol,则溶液中含有铁元素的物质的量为:0.0075mol×2×2=0.03mol,质量为:56g/mol×0.03mol=1.68g>1.12g,所以无机盐M中一定含有Fe元素,无机盐M分子中的原子个数比为2:1:4,则M的化学式为:K2FeO4,
①路线Ⅰ为检验亚铁离子的方法;
②K2FeO4与稀硫酸、铁粉反应生成硫酸亚铁、硫酸钾和水,根据质量守恒可知W为硫酸钾;根据n=$\frac{m}{M}$计算出K2FeO4的物质的量,再根据n=nM计算出钾离子的质量;
③根据K2FeO4与稀硫酸、铁粉反应生成硫酸亚铁、硫酸钾和水写出反应的化学方程式.
解答 解:(1)硫酸是一种重要的含氧酸,实验室用浓硫酸与乙二酸(H2C2O4)晶体共热,可获得CO与CO2的混合气体,再将混合气进一步通过要得到纯净的CO气体,需要除去混合气体中二氧化碳和水,所以应该用碱石灰干燥,
故答案为:碱石灰(CaO或NaOH固体);
(2)优氯净Cl2Na(NCO)3中,钠离子的化合价为+1价,N为-3价、O为-2价、C为+4价,设Cl元素的化合价为x,则:2x+(+1)+3[(-3)+(+4)+(-2)]=0,解得:x=+1;
亚硫酸钠溶液在空气中易变质,则溶液中会存在硫酸根离子,所以判断亚硫酸钠溶液是否变质的方法为:取适量固体于试管,加水溶解,滴加过量盐酸至无气体放出,再滴加BaCl2,有白色沉淀生成证明试样已经变质,
故答案为:+1;取适量固体于试管,加水溶解,滴加过量盐酸至无气体放出,再滴加BaCl2,有白色沉淀生成证明试样已经变质;
(3)①根据路线Ⅰ可知,N溶液中一定含有亚铁离子,
故答案为:Fe2+;
②1.2g氧化铁的物质的量为:$\frac{1.2g}{160g/mol}$=0.0075mol,则溶液中含有铁元素的物质的量为:0.0075mol×2×2=0.03mol,质量为:56g/mol×0.03mol=1.68g>1.12g,所以无机盐M中一定含有Fe元素,无机盐M分子中的原子个数比为2:1:4,则M的化学式为:K2FeO4,根据流程可知,K2FeO4与稀硫酸、还原铁粉反应生成硫酸亚铁和硫酸钾,根据质量守恒可知W为硫酸钾;
1.98gK2FeO4的物质的量为$\frac{1.98g}{198g/mol}$=0.01mol,0.01molK2FeO4中含有0.02mol钾离子,含有钾离子的质量为:39g/mol×0.02mol=0.78g,
故答案为:K2SO4 ;0.78;
③无机盐M与还原铁粉反应生成硫酸亚铁、硫酸钾和水,反应的化学方程式为:2Fe+K2FeO4+4H2SO4═3FeSO4+K2SO4+4H2O,
故答案为:2Fe+K2FeO4+4H2SO4═3FeSO4+K2SO4+4H2O.
点评 本题考查了探究物质组成的方法,题目难度中等,试题涉及物质组成的测定、浓硫酸的性质、离子方程式、化学方程式的书写、离子的检验方法等知识,试题知识点较多、综合性较强,充分考查了学生灵活应用基础知识的能力.


科目:高中化学 来源: 题型:选择题
| A. | 126C和146C是一种核素 | |
| B. | 红磷和白磷互为同素异形体 | |
| C. | CH3COOCH2CH3和CH3CH2COOCH3是不同物质 | |
| D. | CH3CH2OH可看成是由-C2H5和-OH两种基团组成 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
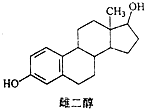
| A. | 能与Na、Na0H溶液、Na2CO3溶液反应 | |
| B. | 能发生加成反应、取代反应、消去反应 | |
| C. | 该分子中所有碳原子不可能在同一个平面内 | |
| D. | 可与FeC13溶液发生显色反应,但不能发生氧化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
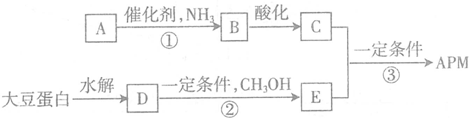
 .C中所含官能团的名称为羧基、氨基.
.C中所含官能团的名称为羧基、氨基. .
.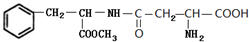 和
和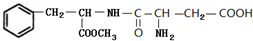 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
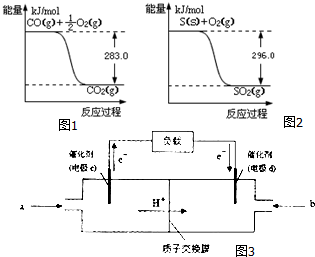 一氧化碳是一种用途广泛的化工基础原料.有机物加氢反应中镍是常用的催化剂.但H2中一般含有微量CO会使催化剂镍中毒,在反应过程中消除CO的理想做法是投入少量SO2,为弄清该方法对催化剂的影响,查得资
一氧化碳是一种用途广泛的化工基础原料.有机物加氢反应中镍是常用的催化剂.但H2中一般含有微量CO会使催化剂镍中毒,在反应过程中消除CO的理想做法是投入少量SO2,为弄清该方法对催化剂的影响,查得资查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 实验目的 |
| A | 将二氧化硫气体通入紫色石蕊试液中,观察溶液颜色变化 | 证明二氧化硫具有漂白性 |
| B | 向2mL 1mol•L-1NaOH溶液中先加入3滴1mol•L-1 FeCl3,再加入3滴1mol•L-1MgCl2溶液 | 证明K[Mg(OH)2]>K[Fe(OH)3] |
| C | 相同条件下,向两支盛有相同体积不同浓度H2O2溶液的试管中分别滴入适量相同浓度的CuSO4溶液和FeCl3溶液 | 探究Cu2+、Fe3+对H2O2分解速率的影响 |
| D | 向2mL品红溶液和2mL加入少许醋酸的品红溶液中分别滴入3滴NaClO的84消毒液,观察红色褪色的快慢 | 证明溶液pH的减少,84消毒液的氧化能力增强 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
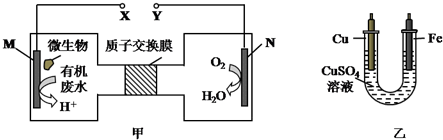
| A. | H十透过质子交换膜由左向右移动 | |
| B. | 铜电极应与Y相连接 | |
| C. | M电极反应式:H2NCONH2+H2O-6e-═CO2↑+N2↑+6H+ | |
| D. | 当N电极消耗0.25 mol气体时,则铁电极增重16g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
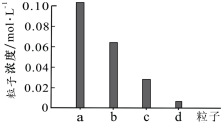 常温下,将0.20mol/L H2X溶液与0.20mol/L NaOH溶液等体积混合,所得溶液pH=3.6,继续滴加NaOH溶液至pH=4.0时,部分粒子浓度如下图所示.下列说法错误的是( )
常温下,将0.20mol/L H2X溶液与0.20mol/L NaOH溶液等体积混合,所得溶液pH=3.6,继续滴加NaOH溶液至pH=4.0时,部分粒子浓度如下图所示.下列说法错误的是( )| A. | 图中a代表Na+,d代表H2X分子 | |
| B. | H2X为二元弱酸,HX-的电离程度大于水解程度 | |
| C. | 混合溶液pH=3.6时:c(H+)+c(H2X)=c(X2-)+c(OH-) | |
| D. | 继续滴加NaOH溶液至pH=7.0时:c(Na+)>c(HX-)+2c(X2-) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
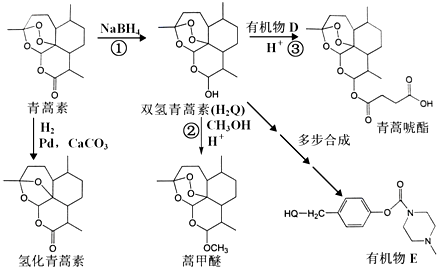
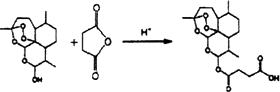 .
.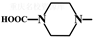 外,还需含苯环的二羟基化合物F,写如有机物F与NaOH溶液反应的离子反应方程式
外,还需含苯环的二羟基化合物F,写如有机物F与NaOH溶液反应的离子反应方程式 ,有机物G是F的同分异构体,有机物G遇FeCl3溶液显紫色,且有4种不同类型的氢,其个数比为3:2:2:1,则符合条件的有机物G的同分异构体有3种.
,有机物G是F的同分异构体,有机物G遇FeCl3溶液显紫色,且有4种不同类型的氢,其个数比为3:2:2:1,则符合条件的有机物G的同分异构体有3种.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com