


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、该反应中还原剂是S2O32- |
| B、H2O参与该反应,且作氧化剂 |
| C、根据该反应可判断氧化性:Cl2>SO42- |
| D、上述反应中,每生成1 molSO42-,可脱去2 mol Cl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
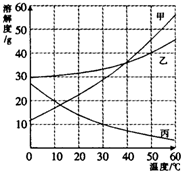 甲、乙、丙三种物质的溶解度曲线如右图所示.据图回答:
甲、乙、丙三种物质的溶解度曲线如右图所示.据图回答:查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温下,18gH2O中含有2NA个氢原子 |
| B、标准状况下,22.4LCCl4含有NA个CCl4分子 |
| C、1mol Na转变成1molNa+会失去2NA个电子 |
| D、0.1 mol?L-1HCl溶液中含有O.1NA个HCl分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com