
 ,已知断裂1mol N-N键吸收167kJ的热量,生成1mol N≡N键放出942kJ热量.试判断相同条件下N4与N2的稳定性顺序是:
,已知断裂1mol N-N键吸收167kJ的热量,生成1mol N≡N键放出942kJ热量.试判断相同条件下N4与N2的稳定性顺序是:

科目:高中化学 来源: 题型:
| A、常温下,SO2、NO2、Cl2均为有刺激性气味、有毒的气体 |
| B、Na2CO3粉末遇水生成含有结晶水的碳酸钠晶体,该晶体一定是Na2CO3?10H2O |
| C、人工合成的硅橡胶是目前最好的、既耐高温又耐低温的橡胶 |
| D、合金的硬度可以大于它的纯金属成分,合金的熔点也可以低于它的成分金属 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
 焦亚硫酸钠(Na2S2O5)是常用的食品抗氧化剂之一.某研究小组进行如下实验:
焦亚硫酸钠(Na2S2O5)是常用的食品抗氧化剂之一.某研究小组进行如下实验:

查看答案和解析>>
科目:高中化学 来源: 题型:
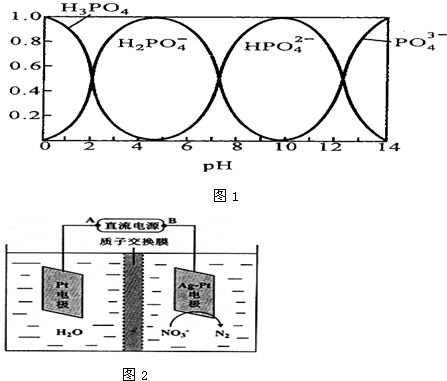
| c(Na+) |
| c(PO43-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、食物放在冰箱中 |
| B、塑料制品中添加抑制剂 |
| C、在糕点包装内放置小包除氧剂 |
| D、燃煤发电时用煤粉代替煤块 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、只有①③ | B、只有①②③ |
| C、只有②③④ | D、有①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
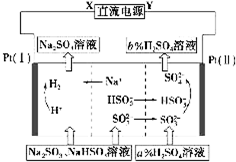 用Na2SO3溶液吸收硫酸工业尾气中的二氧化硫,将所得的混合液进行电解循环再生,这种新工艺叫再生循环脱硫法.其中阴、阳离子交换膜组合循环再生机理如图所示,则下列有关说法中正确的是( )
用Na2SO3溶液吸收硫酸工业尾气中的二氧化硫,将所得的混合液进行电解循环再生,这种新工艺叫再生循环脱硫法.其中阴、阳离子交换膜组合循环再生机理如图所示,则下列有关说法中正确的是( )| A、X为直流电源的正极,Y为直流电源的负极 |
| B、阳极区pH减小 |
| C、图中的b<a |
| D、阴极的电极反应为HSO3--2e-+H2O═SO42-+3H+和SO32--2e-+2H2O═SO42-+4H+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com