
【题目】已知X、Y、Z、W为短周期主族元素,在周期表中的相对位置如图,有下列说法:
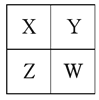
若HmXOn为强酸,则X的氢化物溶于水一定显酸性(m、n均为正整数)
若四种元素均为金属,则Z的最高价氧化物对应的水化物一定为强碱
若四种元素均为非金属,则W的最高价氧化物对应的水化物一定为强酸
④若四种元素只有一定为金属,则Z与Y的最高价氧化物对应的水化物一定为强酸。
其中不正确的说法有几项
A. 1项 B. 2项 C. 3项 D. 4项
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】在容积为1 L的密闭容器中,加入1.0 mol A和2.2 mol B进行如下反应:A(g) + 2B(g) ![]() C(g) + D(g),在800℃时,D的物质的量n(D)和时间t的关系如图。
C(g) + D(g),在800℃时,D的物质的量n(D)和时间t的关系如图。
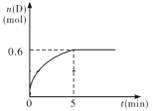
(1)800℃时,0~5 min内,以B表示的平均反应速率为____________。
(2)利用图中数据计算在800 ℃时的平衡常数的数值为___________。
(3)若700℃,反应达平衡时,A的浓度为0.55mol/L,则该反应为_________反应(填“吸热”或“放热”)。
(4)800 ℃时,某时刻测得体系中物质的量浓度如下:c(A)=0.06 mol·L-1,c(B)=0.50 mol·L-1,c(C)=0.20 mol·L-1,c(D)=0.018 mol·L-1,则此时该反应______________(填“向正方向进行”、“向逆方向进行”或“处于平衡状态”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)将等体积等物质的量浓度的醋酸和氢氧化钠溶液混合后,溶液呈 (填“酸性”、“中性”或“碱性”,下同),溶液中c(Na+) c(CH3COO--)(填“>”、“=”或“<”,下同)。
(2)物质的量浓度相同的醋酸和氢氧化钠溶液混合后,溶液中c(Na+) = c(CH3COO--),则混合后溶液呈 ,醋酸体积 氢氧化钠溶液体积。
(3)常温下,pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合后溶液呈 ,溶液中c(Na+) c(CH3COO--)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对①100 mL 0.1 mol/L NaHCO3,②100mL 0.1 mol/L Na2CO3两溶液叙述正确的是( )
A.两溶液中c(OH--):①>②
B.两溶液中阳离子数目:②是①的2倍
C.②溶液中:c(HCO3--)<c(H2CO3)
D.①溶液中:c(CO32-)<c(H2CO3)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近年来,硫化铜矿的湿法冶炼技术已经取得了很大的发展。现有一种催化氧化酸浸硫化铜矿的冶炼法,其工艺流程如图所示:

反应温度、固液比、反应时间、氯离子浓度都对铜的浸出率有较大的影响,下面是实验得出的这几种因素对铜的浸出率影响的变化曲线图(如图~如图所示)。

回答下列问题:
(1)火法炼铜的主要反应:①2CuFeS2+4O2![]() Cu2S+3SO2+2FeO(炉渣);
Cu2S+3SO2+2FeO(炉渣);
②2Cu2S+3O2![]() 2Cu2O+2SO2;③2Cu2O+Cu2S
2Cu2O+2SO2;③2Cu2O+Cu2S![]() 6Cu+SO2↑;则在反应①、②、③中被氧化的元素为_______(填元素符号);若生成的SO2在标准状况下体积为4.48L,则发生转移的电子数目为________NA;由amolCuFeS2生成amolCu,共消耗________molO2。
6Cu+SO2↑;则在反应①、②、③中被氧化的元素为_______(填元素符号);若生成的SO2在标准状况下体积为4.48L,则发生转移的电子数目为________NA;由amolCuFeS2生成amolCu,共消耗________molO2。
(2)写出反应1的化学方程式:________________。经查,硫黄、FeSO4·7H2O均可入药,用途广泛,湿法炼铜与火法炼铜相比,优点是_____________________。
(3)从溶液中得到FeSO4·7H2O晶体的操作是_______________________________。
(4)根据实验以及工业生产的实验要求,从下表中得出的最佳工艺条件为________(填字母代号)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在实验室中手不慎被玻璃划破,可用FeCl3溶液应急止血,其主要原因可能是( )。
A.FeCl3溶液有杀菌消毒作用
B.FeCl3溶液能使血液胶体发生聚沉
C.FeCl3溶液能产生Fe(OH)3沉淀堵住伤口
D.FeCl3能使血液发生化学反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,在元素周期表中处于A,B位置的某些元素性质相似,这称为“对角线规则”.下列有关4号元素铍的性质的推断正确的是( )
A | |
B |
A.铍能与冷水发生剧烈反应
B.氢氧化铍既能与强酸溶液反应,又能与强碱溶液反应
C.氢氧化铍的化学式为Be(OH)3
D.氧化铍只溶于强酸溶液,不溶于强碱溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据要求回答下列问题:
(1)在 ①液氯 ②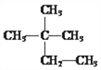 ③白磷 ④氯气
③白磷 ④氯气
⑤![]() ⑥
⑥![]() ⑦
⑦![]() ⑧红磷
⑧红磷
这八种物质中,互为同分异构体的是____,互为同素异形体的是_____。(填序号)
(2)在下列固体中:①CaCl2 ②KOH ③He ④H2SO4 ⑤NH4Cl ⑥金刚石
①其中不含化学键的晶体是_________,
②既含有离子键又含有共价键的物质是______,
③固体熔化时只需破坏共价键的晶体是____(填序号)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究NO2、SO2、CO等大气污染气体的处理具有重要意义。
(1)利用ClO2氧化氮氧化物反应过程如下:
NO![]() NO2
NO2![]() 无污染物
无污染物
反应Ⅰ的化学方程式是2NO+ClO2+H2O=NO2+HNO3+HCl,反应Ⅱ的化学方程式是__________________________。
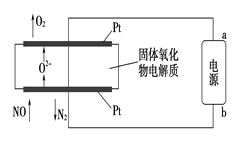
(2)利用固体氧化物电解池通过电解方式分解氮氧化物的过程如图3所示,写出电解池中通入NO一端的电极反应式:_______________________。
(3)已知:2SO2(g)+O2(g)![]() 2SO3(g) ΔH=-196.6 kJ·mol-1
2SO3(g) ΔH=-196.6 kJ·mol-1
2NO(g)+O2(g)![]() 2NO2(g) ΔH=-113.0 kJ·mol-1
2NO2(g) ΔH=-113.0 kJ·mol-1
①则NO2 与SO2反应的热化学方程式为______________________。
②一定条件下,将NO2与SO2以体积比1∶2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是_____________。
a.体系压强保持不变
b.混合气体颜色保持不变
c.SO3和NO的体积比保持不变
d.每消耗1 mol SO3的同时生成1 mol NO2
e.混合气体的平均分子量不再变化
③测得上述反应平衡时NO2与SO2体积比为1∶6,则平衡时NO2的转化率=____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com