
���ֶ���������Ԫ��A��B��C��D��E��ԭ��������������A2������ɫȼ�ϣ�C�������������������ά��DԪ��ԭ�ӵĺ˵������ͬ������һ����Ԫ�ص�2����B��CΪͬ����Ԫ�أ�B��Dԭ������������֮�͵���E�������������� ������������������˵������ȷ����
A. ����Ԫ���������ֽ���Ԫ��
B. Ԫ��C��D��E������������Ӧˮ�����������ǿ
C. Ԫ��D��E�ֱ���Ԫ��A�γɻ�������ȶ��ԣ�A2D>AE
D. Ԫ��B��D��E�ļ����Ӱ뾶��СΪ��B>D>E

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ��ӱ�ʡ��̨�и߶���ѧ�ڵ��Ĵ��¿���ѧ���������棩 ���ͣ�ѡ����
�����£����и���������ָ����Һ���ܴ����������
A��ʹ��̪���ɫ����Һ�У�Na+��A13+��SO42-��Cl-
B��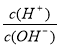 =10����Һ�У�NH4+��Ca2+�� Cl-��NO3-
=10����Һ�У�NH4+��Ca2+�� Cl-��NO3-
C������ˮ�У�Fe2+��K+��NO3-��SO42-
D��ˮ�������c(H+)=1��10-13 mol•L-1����Һ�У�K+��Na+��AlO2-��HCO3-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ��㶫ʡ�����и߶���ѧ����ĩ��ѧ�Ծ��������棩 ���ͣ������
��CO2��CH4��������Ҫ���������壬ͨ��CH4��CO2�ķ�Ӧ���������ֵ�Ļ�ѧƷ��Ŀǰ���о�Ŀ�ꡣ250��ʱ�������Ͻ�Ϊ�������������·�Ӧ��CO2(g)+CH4(g)?2CO (g)+2H2(g)
(g)+2H2(g)
(1)���¶��¸÷�Ӧ��ƽ�ⳣ������ʽK= ��
(2)��֪����CH4(g)+2O2(g)�TCO2(g)+2H2O(g) ��H=��890.3kJ•mol��1
�� CO(g)+H2O(g)�TCO2(g)+H2(g) ��H=+2.8kJ•mol��1
��2CO(g)+O2(g)�T2CO2(g) ��H=��566.0kJ•mol��1
��ӦCO2(g)+CH4(g) 2CO(g)+2H2(g)�ġ�H= kJ•mol��1��
2CO(g)+2H2(g)�ġ�H= kJ•mol��1��
(3)����������Ӧ�����ȼ�ϵ��(�������ҺΪ����������Һ)��д����ظ����ĵ缫��Ӧʽ ��
����Դ��ȱ������������ٵ��ش����⣮�״���һ�ֿ�������Դ�����й㷺�Ŀ�����Ӧ��ǰ������ҵ�Ϻϳɼ״��ķ�Ӧԭ��Ϊ��CO(g)+2H2(g)?CH3OH(g) ��H��
�±����������Ǹ÷�Ӧ�ڲ�ͬ�¶��µĻ�ѧƽ�ⳣ��(K)��
�¶� | 250�� | 300�� | 350�� |
K | 2.041 | 0.270 | 0.012 |
(1)���ݱ������ݿ��жϡ�H 0 (���������=������)��
(2)300��ʱ����2molCO��3molH2��2molCH3OH�����ݻ�Ϊ1L���ܱ������У���ʱ��Ӧ�� (�����)��A�����ƶ� B�����ƶ� C����ƽ��״̬ D���ж�
(3)������˵��������Ӧ�ﵽ��ѧƽ��״̬�ı�־��
A�����º����£����������ܶȲ��ڱ仯
B����ƽ��ʱ��v(CO)��v(H2)��v(CH3OH)=1��2��1
C����ƽ��ʱ��CH3OHŨ�Ȳ��ٱ仯
D����λʱ��������nmolCOͬʱ����2nmolH2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ��㶫ʡ�����и߶���ѧ����ĩ��ѧ�Ծ��������棩 ���ͣ�ѡ����
һ�����ĵ�ϡH2SO4��������۷�Ӧʱ��Ϊ������Ӧ���ʣ��Ҳ�Ӱ������H2������������ϡH2SO4�м���
A��CH3COONa���� B��Na2SO4���� C������NH4HSO4���� D�� NaOH����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�켪�ֳ��������ѧУ��������ĩ��ѧ�Ծ��������棩 ���ͣ������
�״���һ������ȼ�ϣ��ڹ�ҵ�ϳ���CO��H2�ϳɼ״�����Ӧ����ʽΪCO(g)+2H2(g) =CH3OH(g)��

(1)����CO(g)+2H2(g)=CH3OH(g)�ķ�Ӧ�ȡ�H4=____________��
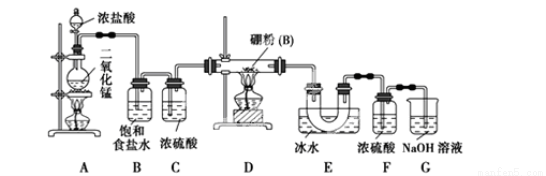
(2)Ϊ�����ȼ�ϵ������ʿ��Խ��״����Ϊȼ�ϵ�أ������Դ�Ϊ��Դ���е��ʵ�飬װ����ͼ��ʾ���ش�������⡣
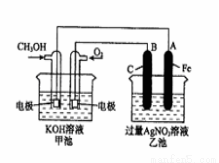
��д��ͨ�״�һ���ĵ缫��Ӧ����ʽ ��д���ҳ���B(C)�缫�ĵ缫��Ӧʽ ��
�ڷ�Ӧ�����У��ҳ���ҺpH�ı仯Ϊ (�� �ߡ����ͻ�)
�۵��ҳ���A(Fe)������������5.40gʱ���׳�������������O2 mL(��״����)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�켪�ֳ��������ѧУ��������ĩ��ѧ�Ծ��������棩 ���ͣ�ѡ����
����ʽΪC5H12O�Ҳ�������Ʒ�Ӧ�ų��������л���������(�����������칹)
A��5�� B��6�� C��7�� D��8��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�����ʡ����1���ʼ컯ѧ�Ծ��������棩 ���ͣ��ƶ���
����ѧ����ѡ��3�����ʽṹ�����ʡ�ԭ������С��36��X��Y��Z��W����Ԫ�أ�����X���γɻ�������������Ԫ�أ�Yԭ�ӻ�̬ʱ���������������ڲ��������2����Zԭ�ӻ�̬ʱ2pԭ�ӹ������3��δ�ɶԵĵ��ӣ�W��ԭ������Ϊ29���ش��������⣺
��1��W+�ĵ����Ų�ʽΪ ��Y2X2������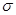 ����м���֮��Ϊ ��
����м���֮��Ϊ ��
��2��������ZX3��YX4��Һ������Ҫԭ���� ��
��3��Ԫ��Y��һ����������Ԫ��Z��һ�������ﻥΪ�ȵ����壬Ԫ��Z��������������ӵĽṹʽ�� ��
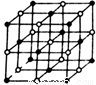
��4��Ԫ��W��һ���Ȼ��ᄃ��ľ����ṹ��ͼ��ʾ�����Ȼ���Ļ�ѧʽ�� ������þ�����ܶ�Ϊd g��cm--3�������ӵ�����ΪNA������������������������������ļ�ľ���Ϊ cm��
��5��ZX3��VSEPR����Ϊ ��ZF3���ӵĿռ乹��Ϊ ��ZX3������W2+�γ������ӣ���ZF3������W2���γ������ӣ���ԭ���� _��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�챱���з�̨��������ѧ����ĩ��ѧ�Ծ��������棩 ���ͣ�ѡ����
�����£���100 mL 0.1 mol/L NH4Cl��Һ�м����������ʡ��йؽ�����ȷ����
��������� | ���� | |
A�� | 100 mL 0.1 mol/L���� | ��Һ��2c(NH4+)= c(Cl��) |
B�� | 0.01 mol Na2O2���� | ��Ӧ��ȫ����ҺpH����c(Na��) = 2c(Cl��) |
C�� | 100 mL H2O | ��ˮ�������c(H��)•c(OH��)���� |
D�� | 100 mL 0.1 mol/L NH3•H2O | ��Һ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�꼪��ʡ���������ظ߶�����ĩ��ѧ�Ծ��������棩 ���ͣ�ѡ����
Li-SOCl2��������������������ȵĵ�ء��õ�����Ϊ������̼��Ϊ��������ˮ��������ﮣ�LiAlCl4����SOCl2��ҺΪ���Һ������ܷ�ӦΪ��ص��ܷ�Ӧ�ɱ�ʾΪ��4Li+2SOCl2= 4LiCl +SO2 +S������˵������ȷ����
A�������ĵ缫��ӦʽΪ Li-e-��Li+
B�������ĵ缫��ӦʽΪ2SOCl2+4e-��SO2+S+4Cl-
C�������Һ�к���ˮ����õ�ص�Ч�ʽ����
D����������14gLi�μӷ�Ӧ����������������·�еĵ�����ԼΪ1.204��1023
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com