
·ÖĪö £Ø1£©2NH3£Øg£©+CO2£Øg£©?NH2COONH4£Øs£©£¬øĆ·“Ó¦ĪŖģŲ¼õµÄ¹ż³Ģ£¬ČōÄÜ×Ō·¢½ųŠŠ£¬ĖµĆ÷øĆ·“Ó¦ĪŖ·ÅČČ·“Ó¦£¬¾Ż“Ė½ā“š¼“æÉ£»
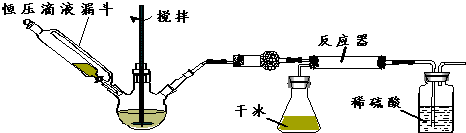
£Ø2£©ŗćŃ¹µĪŅŗĀ©¶·“śĢę·ÖŅŗĀ©¶·æÉŅŌĘ½ŗāÄŚĶāŃ¹Ē棬Ź¹°±Ė®Ė³ĄūµĪĻĀ£»
£Ø3£©·“Ó¦Īļ°±Ęų±ŲŠėŹĒøÉŌļµÄ£¬ŠčŅŖÓĆ¼īŠŌøÉŌļ¼ĮøÉŌļ£¬Čē¼īŹÆ»Ņ”¢¹ĢĢåĒāŃõ»ÆÄĘ»ņŃõ»ÆøĘµČ£»
£Ø4£©ÅØ°±Ė®¼ÓČėĒāŃõ»ÆÄĘ¹ĢĢ壬ĒāŃõ»ÆÄĘ¹ĢĢåČܽā·ÅČČ£¬Ź¹Ņ»Ė®ŗĻ°±·Ö½āÉś³É°±ĘųµÄ»ÆŃ§Ę½ŗāNH3+H2O?NH3•H2O?NH4++OH-£¬ÄęĻņ½ųŠŠ£»
£Ø5£©øɱłÖĘČ”µÄ¶žŃõ»ÆĢ¼ÖŠ²»ŗ¬ŌÓÖŹ£¬²»ŠčŅŖøÉŌļ£»øĆ·“Ó¦ĪŖ·ÅČČ·“Ó¦£¬øɱł±äĪŖ¶žŃõ»ÆĢ¼ĪüŹÕČČĮ棬ӊĄūÓŚŌö“ó·“Ó¦Īļ×Ŗ»ÆĀŹ£»
£Ø6£©·“Ó¦ŗóĘŚ¶žŃõ»ÆĢ¼µÄĮæ¼õÉŁ£¬æÉŅŌ²ÉČ”“ėŹ©ČĆĶØČėµÄ°±ĘųŅ²¼õÉŁ£»
£Ø7£©ŅĄ¾Ż×°ÖĆĶ¼ÖŠĮ÷³Ģ·ÖĪö£¬°²Č«ĪŹĢāÖ÷ŅŖŹĒ¶ĀČūµ¼Ęų¹Ü£¬ŅŗĢå·¢Éśµ¹Īü£»ŅĄ¾Ż·“Ó¦¹ż³ĢÖŠµÄ²śĪļ·ÖĪö£¬²»ÄÜ°ŃĪŪČ¾ŠŌµÄĘųĢåÅŷŵ½æÕĘųÖŠ£¬ĪüŹÕŅ×ČÜÓŚĖ®µÄĘųĢåŠčŅŖ·Åµ¹Īü£®
½ā“š ½ā£ŗ£Ø1£©2NH3£Øg£©+CO2£Øg£©?NH2COONH4£Øs£©£¬øĆ·“Ó¦ĪŖģŲ¼õµÄ¹ż³Ģ£¬ČōÄÜ×Ō·¢½ųŠŠ£¬ĖµĆ÷øĆ·“Ó¦ĪŖ·ÅČČ·“Ó¦£¬¼“”÷H£¼0£¬
¹Ź“š°øĪŖ£ŗŠ”ÓŚ£»
£Ø2£©ŗĶĘÕĶØ·ÖŅŗĀ©¶·Ļą±Č£¬ŗćŃ¹µĪŅŗĀ©¶·ÉĻ²æŗĶČż¾±ÉÕĘæĘųŃ¹ĻąĶØ£¬æÉŅŌ±£Ö¤ŗćŃ¹µĪŅŗĀ©¶·ÖŠµÄŅŗĢåĖ³ĄūµĪĻĀ£¬
¹Ź“š°øĪŖ£ŗŹ¹°±Ė®Ė³ĄūµĪĻĀ£»
£Ø3£©ÓÉÓŚÖʱø°±»ł¼×Ėįļ§µÄŌĮĻ°±Ęų±ŲŠėŹĒøÉŌļµÄ£¬ŅŌ·ĄÖ¹ø±·“Ó¦µÄ·¢Éś£¬Ņņ“ĖÉś³ÉµÄ°±Ęų±ŲŠė½ųŠŠøÉŌļ£¬ŅņĪŖ°±ĘųŹĒ¼īŠŌĘųĢ壬ĖłŅŌøÉŌļ°±ĘųÓ¦øĆÓĆŃõ»ÆøĘ»ņ¹ĢĢåĒāŃõ»ÆÄĘ»ņ¼īŹÆ»Ņ£¬
¹Ź“š°øĪŖ£ŗ¹ĢĢåĒāŃõ»ÆÄĘ»ņ¼īŹÆ»Ņ£»
£Ø4£©ÅØ°±Ė®¼ÓČėĒāŃõ»ÆÄĘ¹ĢĢ壬ĒāŃõ»ÆÄĘ¹ĢĢåČܽā·ÅČČ£¬Ź¹Ņ»Ė®ŗĻ°±·Ö½āÉś³É°±ĘųµÄ»ÆŃ§Ę½ŗāNH3+H2O?NH3•H2O?NH4++OH-£¬ÄęĻņ½ųŠŠ£¬ÄÜÓĆ»ÆŃ§Ę½ŗāŅʶÆŌĄķ½āŹĶ£¬
¹Ź“š°øĪŖ£ŗĒāŃõ»ÆÄĘ¹ĢĢåČܽā·ÅČČŗĶOH-Ź¹Ņ»Ė®ŗĻ°±·Ö½āÉś³É°±ĘųµÄ»ÆŃ§Ę½ŗāNH3+H2O?NH3•H2O?NH4++OH-ÄęĻņ½ųŠŠ£®
£Ø5£©Ģ¼ĖįŃĪŗĶĖį·“Ó¦ÖĘCO2£¬ŌņÉś³ÉµÄCO2±ŲŠė½ųŠŠ¾»»ÆŗĶøÉŌļ“¦Ąķ£¬¶ųÖ±½ÓĄūÓĆøɱłÖʱøCO2£¬²»ŠčŅŖøÉŌļ£»ÓÖŅņĪŖøĆ·“Ó¦ŹĒ·ÅČČ·“Ó¦£¬Ģį¹©µĶĪĀ»·¾³£¬æÉŅŌĢįøß×Ŗ»ÆĀŹ£¬
¹Ź“š°øĪŖ£ŗ²»ŠčŅŖøÉŌļ£»Ģį¹©µĶĪĀ»·¾³£¬Ģįøß×Ŗ»ÆĀŹ£»
£Ø6£©·“Ó¦ŗóĘŚ£¬ÓÉÓŚ¶žŃõ»ÆĢ¼µÄĘųĮ÷ĻĀ½µ£¬µ¼ÖĀĶØČėµÄ¶žŃõ»ÆĢ¼ĘųĢå¼õÉŁ£¬“ĖŹ±æÉŅŌĶعżµ÷½ŚŗćŃ¹µĪŅŗĀ©¶·ŠżČū£¬¼õĀż°±Ė®µÄµĪ¼ÓĖŁ¶Č£¬
¹Ź“š°øĪŖ£ŗµ÷½ŚŗćŃ¹µĪŅŗĀ©¶·ŠżČū£¬¼õĀż°±Ė®µÄµĪ¼ÓĖŁ¶Č£»
£Ø7£©ŅĄ¾Ż×°ÖĆĶ¼ÖŠĮ÷³Ģ·ÖĪö£¬°²Č«ĪŹĢāÖ÷ŅŖŹĒ¶ĀČūµ¼Ęų¹Ü£¬ŅŗĢå·¢Éśµ¹Īü£»ŅĄ¾Ż·“Ó¦¹ż³ĢÖŠµÄ²śĪļ·ÖĪö£¬²»ÄÜ°ŃĪŪČ¾ŠŌµÄĘųĢåÅŷŵ½æÕĘųÖŠ£¬ĪüŹÕŅ×ČÜÓŚĖ®µÄĘųĢåŠčŅŖ·Åµ¹Īü£¬ŹµŃé×°ÖĆ“ęŌŚ°²Č«ĪŹĢā²śĘ·Ņ׶ĀČūµ¼¹Ü£¬Ļ”ĮņĖį»įµ¹Īü£¬
¹Ź“š°øĪŖ£ŗ²śĘ·Ņ׶ĀČūµ¼¹Ü£¬Ļ”ĮņĖį»įµ¹Īü£®
µćĘĄ ±¾Ģāæ¼²éĮĖĪļÖŹÖʱøŹµŃéµÄÉč¼ĘÓ¦ÓĆ£¬Ö÷ŅŖŹĒ°±ĘųµÄÖʱø·½·Ø£¬°±»ł¼×ĖįµÄÖʱøŹµŃé×°ÖĆ·ÖĪöÅŠ¶Ļ£¬ŹµŃ黳±¾²Ł×÷£¬»ģŗĻĪļ·ÖĄėµÄŹµŃéÉč¼Ę£¬ĢāÄæÄѶČÖŠµČ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
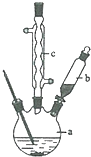 ±½ŅŅĖįĶŹĒŗĻ³ÉÓÅĮ¼“߻ƼĮ”¢“«øŠ²ÄĮĻ--ÄÉĆ×Ńõ»ÆĶµÄÖŲŅŖĒ°ĒżĢåÖ®Ņ»£®ĻĀĆęŹĒĖüµÄŅ»ÖÖŹµŃéŹŅŗĻ³ÉĀ·Ļߣŗ
±½ŅŅĖįĶŹĒŗĻ³ÉÓÅĮ¼“߻ƼĮ”¢“«øŠ²ÄĮĻ--ÄÉĆ×Ńõ»ÆĶµÄÖŲŅŖĒ°ĒżĢåÖ®Ņ»£®ĻĀĆęŹĒĖüµÄŅ»ÖÖŹµŃéŹŅŗĻ³ÉĀ·Ļߣŗ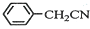 +H2O+H2SO4$\stackrel{100”«130”ę}{”ś}$
+H2O+H2SO4$\stackrel{100”«130”ę}{”ś}$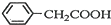 +NH4HSO4
+NH4HSO4 +Cu£ØOH£©2”ś£Ø
+Cu£ØOH£©2”ś£Ø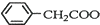 £©2Cu+H2O
£©2Cu+H2O²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
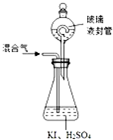 ¶žŃõ»ÆĀČ£ØClO2£¬»ĘĀĢÉ«Ņ×ČÜÓŚĖ®µÄĘųĢ壩ŹĒøߊ§”¢µĶ¶¾µÄĻū¶¾¼Į£¬»Ų“šĻĀĮŠĪŹĢā£ŗ
¶žŃõ»ÆĀČ£ØClO2£¬»ĘĀĢÉ«Ņ×ČÜÓŚĖ®µÄĘųĢ壩ŹĒøߊ§”¢µĶ¶¾µÄĻū¶¾¼Į£¬»Ų“šĻĀĮŠĪŹĢā£ŗ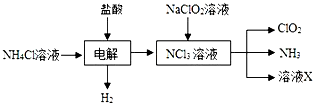
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | CxHy£Øl£©+£Øx+$\frac{y}{4}$£©O2£Øg£©=xCO2£Øg£©+$\frac{y}{2}$H2O£Øl£©”÷H=£Ø$\frac{10Q}{9}$-1366.8£©kJ•mol-1 | |
| B£® | CxHy£Øl£©+£Øx+$\frac{y}{4}$£©O2£Øg£©=xCO2£Øg£©+$\frac{y}{2}$H2O£Øl£©”÷H=£Ø-$\frac{10Q}{9}$+1366.8£©kJ•mol-1 | |
| C£® | CxHy£Øl£©+£Øx+$\frac{y}{4}$£©O2£Øg£©=xCO2£Øg£©+$\frac{y}{2}$H2O£Øl£©”÷H=£Ø$\frac{10Q}{9}$-151.9£©kJ•mol-1 | |
| D£® | CxHy£Øl£©+£Øx+$\frac{y}{4}$£©O2£Øg£©=xCO2£Øg£©+$\frac{y}{2}$H2O£Øl£©”÷H=£Ø-$\frac{10Q}{9}$+151.9£©kJ•mol-1 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
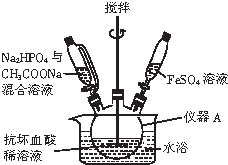 Į×ĖįŃĒĢś¾§Ģå[Fe3£ØPO4£©2•8H2O]ŹĒĄ¶°×É«µ„Š±¾§Ģ壬ČÜÓŚĻ”ĒæĖį£¬²»ČÜÓŚĖ®”¢“×Ėį”¢“¼£¬Ö÷ŅŖÓĆÓŚÖĘ×÷Į×ĖįĢśļ±µē³Ų£®ŹµŃéŹŅÖʱøĮ×ĖįŃĒĢś¾§ĢåµÄ×°ÖĆ”¢·“Ó¦ŌĄķŗĶŹµŃé²½ÖčČēĻĀ£ŗ
Į×ĖįŃĒĢś¾§Ģå[Fe3£ØPO4£©2•8H2O]ŹĒĄ¶°×É«µ„Š±¾§Ģ壬ČÜÓŚĻ”ĒæĖį£¬²»ČÜÓŚĖ®”¢“×Ėį”¢“¼£¬Ö÷ŅŖÓĆÓŚÖĘ×÷Į×ĖįĢśļ±µē³Ų£®ŹµŃéŹŅÖʱøĮ×ĖįŃĒĢś¾§ĢåµÄ×°ÖĆ”¢·“Ó¦ŌĄķŗĶŹµŃé²½ÖčČēĻĀ£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ļرČĆ¾½šŹōŠŌĒæ | |
| B£® | ĀČ»ÆĆ¾±ČĀČ»ÆļØÄŃČÜ | |
| C£® | øßĪĀĻĀ£¬Ć¾Ąė×ӵƵē×ÓÄÜĮ¦±ČļØĄė×ÓČõ | |
| D£® | ļصķŠµć±ČĆ¾µĶ£¬µ±°ŃļØÕōĘų³é×ߏ±£¬Ę½ŗāĻņÓŅ·“Ó¦·½ĻņŅĘ¶Æ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | C8H18£Øl£©+$\frac{25}{2}$O2£Øg£©ØT8CO2£Øg£©+9H2O£Øg£©”÷H=-48.4 kJ•mol-1 | |
| B£® | C8H18£Øl£©+$\frac{25}{2}$O2£Øg£©ØT8CO2£Øg£©+9H2O£Øl£©”÷H=-5517.6 kJ•mol-1 | |
| C£® | C8H18£Øl£©+$\frac{25}{2}$O2£Øg£©ØT8CO2£Øg£©+9H2O£Øl£©”÷H=+5517.6 kJ•mol-1 | |
| D£® | C8H18£Øl£©+$\frac{25}{2}$O2£Øg£©ØT8CO2£Øg£©+9H2O£Øl£©”÷H=-48.4 kJ•mol-1 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com