
 (1)高铁电池是一种新型可充电电池,与普通电池相比,该电池能较长时间保持稳定的放电电压.高铁电池的总反应为:
(1)高铁电池是一种新型可充电电池,与普通电池相比,该电池能较长时间保持稳定的放电电压.高铁电池的总反应为:分析 (1)①放电时,该电池是原电池,原电池负极上失电子化合价升高而发生氧化反应;
②放电时,正极上得电子发生还原反应,总反应方程式减去负极电极反应式即得正极反应式;
③根据电极反应式确定碱性增强的电极;
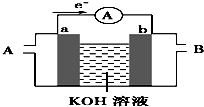
(2)①由电子转移方向可知a为负极,发生氧化反应,应通入燃料,b为正极,发生还原反应,应通入空气;
②假设使用的“燃料”是甲烷,则负极发生CH4-8e-+10OH-═CO+7H2O;
根据负极上的反应,消耗负极质量减少一样多时,转移得电子的物质的量即可;
解答 解:(1)①电池的负极上发生氧化反应,正极上发生还原反应.由高铁电池放电时总反应方程式可知,负极材料应为作还原剂的Zn,故答案为:锌;
②正极上得电子发生还原反应,由电池的总反应方程式-负极反应式=正极反应式可知,正极反应式为FeO42-+3e-+4H2O═Fe(OH)3+5OH-,
故答案为:还原;FeO42-+3e-+4H2O═Fe(OH)3+5OH-;
③放电时,负极电极反应式为Zn-2e-+2OH-═Zn(OH)2,正极反应式为FeO42-+3e-+4H2O═Fe(OH)3+5OH-,根据电极反应式知,正极上生成氢氧根离子导致溶液中氢氧根离子浓度增大,溶液的PH增大,
故答案为:正;
(2)①由电子转移方向可知a为负极,发生氧化反应,应通入燃料,b为正极,发生还原反应,应通入空气,故答案为:B;
②假设使用的“燃料”是甲烷,则负极发生CH4-8e-+10OH-═CO+7H2O,故答案为:②CH4-8e-+10OH-═CO+7H2O;
根据负极上的电极反应式:CH4-8e-+10OH-═CO+7H2O,消耗1g甲烷,转移电子的物质的量是$\frac{8}{16}$mol,铅蓄电池的负极上发生的反应为:Pb-2e-+SO42-=PbSO4,
消耗1gPb,转移电子的物质的量是$\frac{2}{207}$mol,所以当消耗相同质量的负极活性物质时,甲烷燃料电池的理论放电量是铅蓄电池的比值是$\frac{8}{16}$mol:$\frac{2}{207}$mol=51.8,故答案为:51.8.
点评 本题考查了原电池原理以及燃料电池的应用,根据元素化合价变化来确定正负极,在书写电池的电极方程式时要注意电解质对反应产物的影响,难度不大.


科目:高中化学 来源: 题型:解答题


查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 要鉴别己烯中是否混有少量甲苯,应先加足量溴水,然后再加入酸性高锰酸钾溶液 | |
| B. | 配制浓硫酸和浓硝酸的混酸时,将浓硝酸沿壁缓缓倒入到浓硫酸中 | |
| C. | 制硝基苯时,将盛有混合液的试管直接在酒精灯火焰上加热 | |
| D. | 除去溴苯中少量的溴,可以加水后分液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
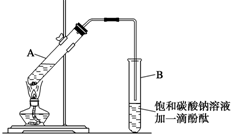 已知下表所示数据:
已知下表所示数据:| 物质 | 熔点(℃) | 沸点(℃) | 密度(g•cm-3) |
| 乙醇 | -117.3 | 78.5 | 0.79 |
| 乙酸 | 16.6 | 117.9 | 1.05 |
| 乙酸乙酯 | -83.6 | 77.5 | 0.90 |
| 浓硫酸 | 338.0 | 1.84 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | a+3b | B. | $\frac{a}{2}$+3b | C. | $\frac{a}{2}$+3b+$\frac{7w}{2}$ | D. | $\frac{a}{2}$+3b-$\frac{7w}{2}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | P4(白磷、s)+3O2(g)═2P2O3(s)△H=-1638 kJ/mol | |
| B. | CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-802.3 kJ/mol | |
| C. | 2CO(g)+O2(g)═2CO2(g)△H=-566 kJ/mol | |
| D. | H2(g)+1/2O2(g)═H2O(l)△H=-285.8 kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Zn与盐酸反应 | B. | CaO与H2O反应 | C. | NaOH与盐酸反应 | D. | C和H2O(g)反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | Al2O3$→_{△}^{NaOH(aq)}$NaAlO2(aq)$\stackrel{CO_{2}}{→}$Al(OH)3 | |
| B. | 饱和NaCl(aq)$\stackrel{NH_{3},CO_{2}}{→}$Na2CO3 | |
| C. | Fe2O3$\stackrel{HCl(aq)}{→}$FeCl3(aq)$\stackrel{△}{→}$无水FeCl3 | |
| D. | MgCl2(aq)$\stackrel{石灰乳}{→}$Mg(OH)2$\stackrel{煅烧}{→}$MgO |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com