
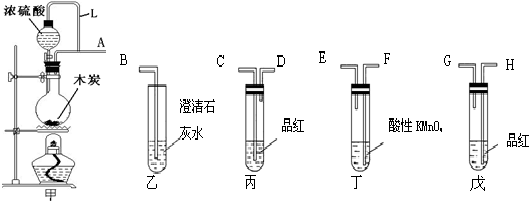
分析 木炭可被浓H2SO4氧化成CO2,由装置可知,甲中发生C与浓硫酸反应生成二氧化碳、二氧化硫,先用品红检验有二氧化硫生成,然后通过高锰酸钾除去二氧化硫,再通过品红,利用品红不褪色说明二氧化硫除尽,最后通过石灰水,石灰水变浑浊,说明有二氧化碳生成,
(1)据气体的性质确定反应装置的连接顺序;
(2)二氧化碳、二氧化硫都能使石灰水变浑浊,先检验二氧化硫,再除去除尽二氧化硫,最后检验二氧化碳;
(3)装置甲中L管平衡气压,保持浓硫酸流下;
(4)高锰酸钾能和二氧化硫反应,但是不和二氧化碳之间反应;
(5)浓硫酸与碳在加热条件下反应生成二氧化碳和二氧化硫和水.
解答 解:木炭可被浓H2SO4氧化成CO2,由装置可知,甲中发生C与浓硫酸反应生成二氧化碳、二氧化硫,先用品红检验有二氧化硫生成,然后通过高锰酸钾除去二氧化硫,再通过品红,利用品红不褪色说明二氧化硫除尽,最后通过石灰水,石灰水变浑浊,说明有二氧化碳生成,
(1)据气体的性质和装置目的,确定反应装置的连接顺序是ACDFEHGB;故答案为:CDFEHGB;
(2)浓硫酸与碳在加热条件下反应生成二氧化碳和二氧化硫和水,二氧化碳、二氧化硫都能使石灰水变浑浊,先检验二氧化硫,再除去除尽二氧化硫,最后检验二氧化碳,丙中品红未褪色,乙中出现白色沉淀,表明已检验出CO2,故答案为:SO2;乙中出现白色沉淀,丙中品红未褪色;
(3)装置甲中L管平衡气压,保持浓硫酸流下,故答案为:平衡气压,保持浓硫酸流下;
(4)高锰酸钾能和二氧化硫反应,但是不和二氧化碳之间反应,丁中酸性KMnO4溶液的作用是除二氧化硫,防止对二氧化碳的验证产生干扰;故答案为:除二氧化硫,防止对二氧化碳的验证产生干扰;
(5)浓硫酸与碳在加热条件下反应生成二氧化碳和二氧化硫和水,即C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O,故答案为:C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O.
点评 本题考查浓硫酸的性质,为高频考点,题目难度中等,把握反应原理、物质的性质、实验装置的作用为解答的关键,侧重学生的分析分析与实验能力的考查.


 星级口算天天练系列答案
星级口算天天练系列答案科目:高中化学 来源: 题型:选择题
| A. | 活化分子之间发生的碰撞一定为有效碰撞 | |
| B. | 升高温度,一般可使活化分子的百分数增大,因而反应速率增大 | |
| C. | 对有气体参加的化学反应增大压强体系体积减小,可使单位体积内活化分子数增加,因而反应速率增大 | |
| D. | 加入适宜的催化剂,可使活化分子的百分数大大增加,从而成千上万倍地增大化学反应的速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
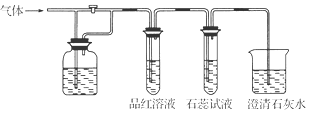
| A. | H2S和浓H2SO4 | B. | SO2和NaHCO3溶液 | C. | Cl2和NaHCO3溶液 | D. | Cl2和氯水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 13:8 | B. | 8:13 | C. | 16:9 | D. | 9:16 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaNO2是氧化剂 | B. | NaNO2在反应中失电子 | ||
| C. | NH4Cl中的N元素被还原 | D. | N2既是氧化剂又是还原剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
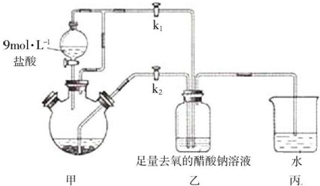
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 新制氯水可使pH试纸先变红,后褪色 | |
| B. | 氯水放置数天后,溶液的酸性逐渐减弱 | |
| C. | 新制的氯水只含Cl2和H2O分子 | |
| D. | 光照氯水有气泡逸出,该气体是Cl2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com