
| A. | 油脂、淀粉、麦芽糖和蛋白质在一定条件都能发生水解反应 | |
| B. | 甲烷和苯都不能与溴水、酸性高锰酸钾溶液发生反应,但苯不属于饱和烃 | |
| C. | 将红热的铜丝迅速插入乙醇中,可观察到铜丝表面变红 | |
| D. | 苯、甲苯、二甲苯等有机物可通过煤的液化、气化后分离获得 |
分析 A.油脂含-COOC-,淀粉为多糖,麦芽糖为二糖,蛋白质含-CONH-;
B.苯、甲烷均不含碳碳双键,苯含苯环;
C.Cu氧化生成CuO,CuO可氧化乙醇;
D.煤的液化生成甲醇、煤的气化生成CO和氢气.
解答 解:A.油脂、淀粉、麦芽糖和蛋白质在一定条件都能发生水解反应,水解产物分别为甘油和高级脂肪酸或盐、葡萄糖、葡萄糖、氨基酸,故A正确;
B.甲烷和苯都不含双键和三键所以都不能与溴水和酸性高锰酸钾反应,甲烷属于饱和烷烃,苯中碳原子未达到最大连接方式,属于不饱和烃,故B正确;
C.乙醇和红热的氧化铜反应生成有刺激性气味的乙醛,黑色氧化铜被还原为红色的铜,故C正确;
D.煤中不含苯和甲苯,通过煤的干馏制得而不是气化和液化,故D错误;
故选D.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系、有机反应为解答的关键,侧重分析与应用能力的考查,注意有机反应类型的判断,题目难度不大.


科目:高中化学 来源: 题型:解答题
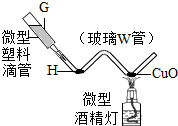 化学实验是进行科学探究的重要方式,基本的化学实验技能是学习化学和进行探究活动的基础和保证.根据要求回答下列问题.
化学实验是进行科学探究的重要方式,基本的化学实验技能是学习化学和进行探究活动的基础和保证.根据要求回答下列问题.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH2=CH2+HOCl→HOCH2-CH2Cl | |
| B. |  +HNO3$→_{△}^{浓硫酸}$ +HNO3$→_{△}^{浓硫酸}$ +H2O +H2O | |
| C. | 2CH3CH2OH+O2 $→_{△}^{Cu}$2CH3CHO+2H2O | |
| D. | C12H22O11+H2O $→_{△}^{稀H_{2}SO_{4}}$ C6H12O6+C6H12O6 蔗糖 葡萄糖 果糖 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaCl、H2O、CO2、H2S | B. | Ne、NH3、P2O5、H2SO4 | ||
| C. | Na2SO4、NH4NO3、PH3、H2S | D. | Si、S、SO2、CO |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 +O2$→_{△}^{Cu}$2
+O2$→_{△}^{Cu}$2 +2H2O.
+2H2O. .
. CH2OCH2CH2CHO B.
CH2OCH2CH2CHO B. CH=CHCH2CH2CHO
CH=CHCH2CH2CHO COOCH2CH2CH3 D.CH2=CHCH=CHCH=CHCH=CHCOOH.
COOCH2CH2CH3 D.CH2=CHCH=CHCH=CHCH=CHCOOH.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 短周期主族元素A、B、C、D、E,原子序数依次增大,A元素的单质常温常温下是最轻的气体,B元素所形成化合物种类最多,C的最高价氧化物对应水化物民其气态氢化物乙能够化合形成盐丙;D元素的离子半径是同周期元素形成的简单离子中最小的.
短周期主族元素A、B、C、D、E,原子序数依次增大,A元素的单质常温常温下是最轻的气体,B元素所形成化合物种类最多,C的最高价氧化物对应水化物民其气态氢化物乙能够化合形成盐丙;D元素的离子半径是同周期元素形成的简单离子中最小的.
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | N2、H2不再化合 | |
| B. | N2、H2、NH3的质量相等 | |
| C. | N2、H2、NH3浓度不再变化 | |
| D. | 改变条件,N2、H2、NH3的浓度也不再变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 二氧化碳的晶胞如图,每8个CO2构成立方体,且在6个面的中心各有1个,在每个CO2周围距离为$\frac{\sqrt{2}}{2}$a(其中a为立方体棱长)的CO2有( )
二氧化碳的晶胞如图,每8个CO2构成立方体,且在6个面的中心各有1个,在每个CO2周围距离为$\frac{\sqrt{2}}{2}$a(其中a为立方体棱长)的CO2有( )| A. | 4个 | B. | 8个 | C. | 12个 | D. | 6个 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com