
| A. | 室温下,1LpH=13的NaOH溶液中,由水电离的OH-数目为0.1NA | |
| B. | 0.1mol${\;}_{38}^{90}$Sr原子中含中子数为3.8NA | |
| C. | 50mL12mol/L的盐酸与足量MnO2共热,转移电子数为0.3NA | |
| D. | 2.0gH218O与D216O的混合物中所含中子数为NA |
分析 A.氢氧化钠溶液中,氢氧根离子抑制了水的电离,则水电离的氢氧根离子浓度=氢离子浓度;
B.质量数=质子数+中子数;
C.二氧化锰只能与浓盐酸反应,和稀盐酸不反应;
D.物质的量n=$\frac{m}{M}$,质量数=质子数+中子数计算分析.
解答 解:A.氢氧化钠溶液中,氢氧根离子抑制了水的电离,溶液中的氢离子是水电离的,则水电离的氢氧根离子浓度=氢离子浓度=1×10-13mol/L,故A错误;
B.原子中含中子数=0.1mol(90-38)×NA=5.2NA,故B错误;
C.二氧化锰只能与浓盐酸反应,和稀盐酸不反应,即盐酸不能反应完全,故转移的电子数小于0.3NA个,故C错误;
D.2.0gH218O物质的量n=$\frac{2.0g}{20g/mol}$=0.1mol,中子数=0.1mol(0+18-8)×NA=NA,D216O的物质的量=$\frac{2.0g}{20g/mol}$=0.1mol,2.0gH218O与D216O的混合物中所含中子数为NA,故D正确;
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,注意二氧化锰和浓盐酸反应,随浓度减小不能生成氯气,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 金属钠长期露置在空气中,最终生成碳酸钠,中间有Na2O2生成 | |
| B. | 比较去锈的铁钉和去锈的绕有细铜丝的铁钉与同浓度盐酸反应速率快慢时,可以加几滴KSCN溶液,观察铁钉周围出现出现血红色现象的快慢 | |
| C. | 原电池的制作:用导线把二极管和锌片、铜片连接起来,锌与铜之间隔一块薄海绵放入稀H2SO4 溶液,二极管发光但很快变暗,若再加入H2O2瞬间又变亮且能持续较长时间 | |
| D. | 在蔗糖中滴加浓硫酸产生的气体,能使酸性KMnO4溶液褪色,说明该气体具有漂白性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
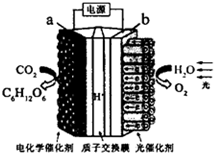
| A. | a极与电源的正极相连 | |
| B. | 该装置能量转化形式仅为电能转化为化学能 | |
| C. | 阳极反应为 6COz+24H+-24e-=C6Hl206+6H20 | |
| D. | 电解后阳极区溶液的pH不变(忽略体积影响) |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 石油的蒸馏实验中,加入碎瓷片可防止石油在蒸馏时暴沸 | |
| B. | 乙醇的催化氧化实验中铜丝主要起氧化剂的作用 | |
| C. | 制取乙酸乙酯时,试剂加入的顺序是:先加入乙醇,后慢慢加入乙酸,最后加入浓硫酸 | |
| D. | 在淀粉溶液中加入少量稀硫酸,水浴加热后,再加入少量新制的氢氧化铜悬浊液,加热至沸腾,没有砖红色沉淀生成,说明淀粉没有水解 | |
| E. | 除去甲烷中混有的少量乙烯,可以将混合气体通过酸性溶KMnO4液 | |
| F. | 用钠可以检验某无水酒精中是否含有水 | |
| G. | 可用溴水来鉴别植物油和矿物油 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题

 (R、R′为烃基)
(R、R′为烃基)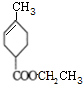 ,D的化学式为C8H11O2Na.
,D的化学式为C8H11O2Na.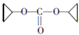 .
. .
.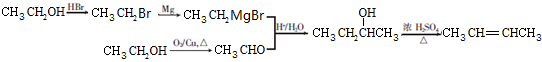 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 16O2与18O2互为同素异形体 | |
| B. | Na2S的电子式为: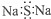 | |
| C. | 熔融状态下硫酸氢钾的电离方程式:KHSO4=K++H++SO42- | |
| D. | 钢铁表面常常出现的铁锈的主要成分是Fe2O3•xH2O,它不能阻止钢铁继续腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
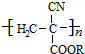 从而具有胶黏性.某种氰基丙烯酸酯(G)的合成路线如下:
从而具有胶黏性.某种氰基丙烯酸酯(G)的合成路线如下: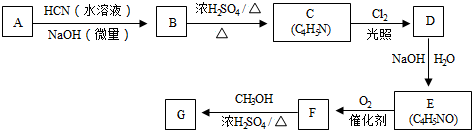
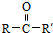 $→_{NaOH(微量)}^{HCN(水溶液)}$
$→_{NaOH(微量)}^{HCN(水溶液)}$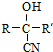
 .其核磁共振氢谱显示为2组峰,峰面积比为1:6.
.其核磁共振氢谱显示为2组峰,峰面积比为1:6. +NaOH$→_{△}^{水}$
+NaOH$→_{△}^{水}$ +NaCl.
+NaCl.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
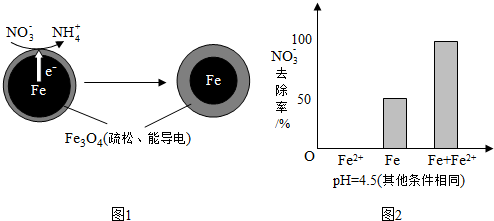
| 初始pH | pH=2.5 | pH=4.5 |
| NO3-的去除率 | 接近100% | <50% |
| 24小时pH | 接近中性 | 接近中性 |
| 铁的最终物质形态 | 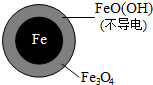 |  |
| 初始pH | pH=2.5 | pH=4.5 |
| NO3-的去除率 | 约10% | 约3% |
| 1小时pH | 接近中性 | 接近中性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com