
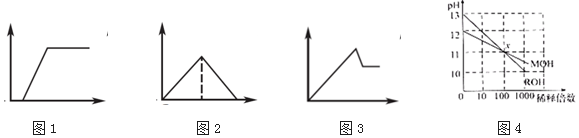
| A. | 图1:往Na2CO3和NaOH混合液中逐滴加入盐酸,产生气体体积与盐酸的物质的量的关系 | |
| B. | 图2:往澄清石灰水中通入过量CO2气体,产生沉淀质量与CO2的物质的量的关系 | |
| C. | 图3:往AlCl3和MgCl2混合液中逐滴加入NaOH溶液,产生沉淀质量与NaOH溶液的物质的量的关系 | |
| D. | 图4:若MOH和ROH表示两种一元碱,则ROH的碱性强于MOH |
分析 A、发生反应:NaOH+HCl═NaCl+H2O、HCl+Na2CO3=NaHCO3+NaCl,后阶段发生反应:NaHCO3+HCl═NaCl+H2O+CO2↑,由此分析解答;
B、沉淀达到最大,反应的方程式为:CO2+Ca(OH)2=CaCO3↓+H2O,溶液又变澄清,反应的方程式为:CO2+CaCO3+H2O=Ca(HCO3)2,消耗二氧化碳的量相等;
C、AlCl3和MgCl2的混合溶液中,逐滴加入NaOH溶液,发生反应生成氢氧化铝、氢氧化镁沉淀,反应的离子方程式为:Al3++3OH-=Al(OH)3↓; Mg2++2OH-=Mg(OH)2↓,随氢氧化钠的加入又发生氢氧化铝溶解于氢氧化钠过程,离子方程式为:Al(OH)3+OH-=AlO2-+2H2O;
D、MOH开始的pH=12,稀释100倍pH=11,则MOH为弱碱.
解答 解:A、发生反应:NaOH+HCl═NaCl+H2O、HCl+Na2CO3=NaHCO3+NaCl,后阶段发生反应:NaHCO3+HCl═NaCl+H2O+CO2↑,所以从开始到产生气体的量应大于产生气体到气体最大量,故A不符合;
B、沉淀达到最大,反应的方程式为:CO2+Ca(OH)2=CaCO3↓+H2O,溶液又变澄清,反应的方程式为:CO2+CaCO3+H2O=Ca(HCO3)2,消耗二氧化碳的量相等,故B符合;
C、AlCl3和MgCl2的混合溶液中,逐滴加入NaOH溶液,发生反应生成氢氧化铝、氢氧化镁沉淀,反应的离子方程式为:Al3++3OH-=Al(OH)3↓; Mg2++2OH-=Mg(OH)2↓,随氢氧化钠的加入又发生氢氧化铝溶解于氢氧化钠过程,离子方程式为:Al(OH)3+OH-=AlO2-+2H2O,故C符合;
D、MOH开始的pH=12,稀释100倍pH=11,则MOH为弱碱,所以ROH的碱性强于MOH,故D符合;
故选A.
点评 本题考查图象问题和弱电解质的电离,明确图象中pH的变化及交点的意义是解答本题的关键,题目难度中等.


 一卷搞定系列答案
一卷搞定系列答案 名校作业本系列答案
名校作业本系列答案 轻巧夺冠周测月考直通名校系列答案
轻巧夺冠周测月考直通名校系列答案科目:高中化学 来源: 题型:实验题
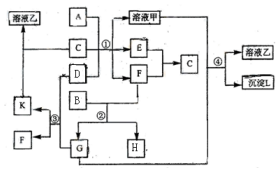 如图表示常见的单质及其化合物之间的转化关系,其中A为常见的金属单质,B为非金属单质(一般是黑色粉末),C是常见的无色无味液体,D是淡黄色的固体化合物.(反应条件图中已省略).
如图表示常见的单质及其化合物之间的转化关系,其中A为常见的金属单质,B为非金属单质(一般是黑色粉末),C是常见的无色无味液体,D是淡黄色的固体化合物.(反应条件图中已省略).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 编号 | 化学反应 | 离子方程式 | 评价 |
| A | 碳酸钙与盐酸 | CO32-+2H+=H2O+CO2↑ | 错误,碳酸钙是弱电解质,不应写成离子形式 |
| B | 向次氯酸钙溶液通入过量CO2 | Ca2++2ClO-+CO2+H2O=CaCO3↓+2HClO | 正确 |
| C | 石灰水中滴加少量NaHCO3溶液 | Ca2++HCO3-+OH-=CaCO3↓+H2O | 错误,不满足Ca(OH)2的配比 |
| D | 过量铁屑溶于稀硝酸 | 3Fe+8H++2NO3-=3Fe2++2NO↑+4H2O | 正确 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
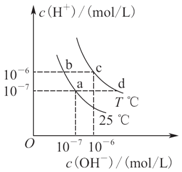
| A. | a点对应的溶液和c点对应的溶液pH大小:pH(c)>pH(a) | |
| B. | 如b点对应的溶液中只含NaHA,则溶液中粒子浓度大小:c(HA-)>c(H2A)>c(H+)>c(A2-) | |
| C. | 25℃时,Ka(HF)=3.6×10-4,Ka(CH3COOH)=1.75×10-5,0.1 mol/L的NaF溶液与0.1 mol/L的CH3COOK溶液相比: c(Na+)-c(F-)>c(K+)-c(CH3COO-) | |
| D. | d点对应的溶液中可大量存在:K+、Ba2+、NO3-、I- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若m=1,则M(NO3)m溶液和氨水互滴时的现象可能不同 | |
| B. | 若m=2,则在空气中蒸干、灼烧MSO4溶液一定能得到MSO4 | |
| C. | 若m=3,则MCl3与足量氢氧化钠溶液反应一定生成M(OH)m | |
| D. | Mm+离子一定不能与酸反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  量取20.00 mL Na2CO3溶液 | B. |  能证明非金属性 Cl>C>Si | ||
| C. | 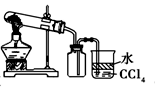 实验室制取并收集NH3 | D. | 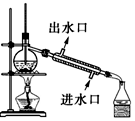 分离酒精与CCl4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由水电离的c(H+):①=②>③=④ | |
| B. | 将②、③两种溶液混合后,若pH=7,则消耗溶液的体积:②=③ | |
| C. | 等体积的①、②两种溶液分别与足量铝粉反应,生成H2的量相等 | |
| D. | 向等体积四种溶液中分别加水至体积为原来的100倍后,溶液的pH:③>④>②>① |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化剂只有硝酸钾 | |
| B. | C即是氧化剂也是还原剂 | |
| C. | 被氧化与被还原的S的质量之比为3:2 | |
| D. | 还原产物只有一种 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com