
| A、1000mL,38.0g |
| B、1000mL,40.0g |
| C、任意规格,38.0g |
| D、500mL,20.0g |


 口算题天天练系列答案
口算题天天练系列答案科目:高中化学 来源: 题型:
 NO3-+
NO3-+ ═
═ Fe2++
Fe2++ NH4++
NH4++
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、C2H4 |
| B、C4H8 |
| C、C4H10 |
| D、C5H10 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、等质量的铝分别与足量氢氧化钠溶液和稀硝酸反应,放出的氢气一样多 |
| B、将SO2通入过量Ba(NO3)2溶液可生成BaSO4沉淀 |
| C、自来水厂常用明矾对水进行杀菌、消毒 |
| D、将稀硫酸滴加到Fe(NO3)2溶液中无明显现象 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
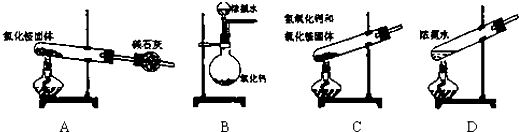
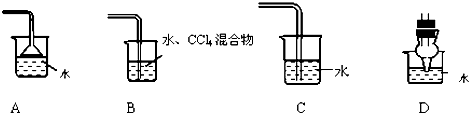
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加入AgNO3溶液,生成白色沉淀,加入稀盐酸沉淀不溶解,可确定有Cl-存在 |
| B、加入稀盐酸,产生的气体能使澄清石灰水变浑浊,可确定有CO32-存在 |
| C、加入BaCl2溶液产生白色沉淀,再加入足量稀盐酸沉淀不溶解,确定有SO42-存在 |
| D、加入BaCl2溶液产生白色沉淀,加入稀硝酸沉淀溶解,并产生无色无味气体,且能使澄清石灰水变浑浊,确定含有CO32-离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、某学生用pH试纸测新制氯水的pH值,先变红后褪色,是因为Cl2有强氧化性 |
| B、向氯水中加入碳酸氢钠粉末,有气泡产生,说明氯水中含有H+ |
| C、配制一定物质的量浓度的溶液发现浓度偏低,可能由于配制溶液所用的容量瓶事先未干燥 |
| D、将铜片放入浓硫酸中,无明显实验现象,说明铜在冷的浓硫酸中发生钝化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
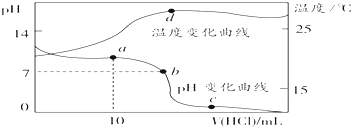 室温下,将1.00mol?L-1盐酸滴入20.00mL 1.00mol?L-1的氨水中,溶液pH和温度随加入盐酸体积的变化曲线如图所示.下列有关说法中不正确的是( )
室温下,将1.00mol?L-1盐酸滴入20.00mL 1.00mol?L-1的氨水中,溶液pH和温度随加入盐酸体积的变化曲线如图所示.下列有关说法中不正确的是( )| A、a点溶液中离子浓度大小关系:c(NH4+)>c(Cl-)>c(OH-)>c(H+) |
| B、b点溶液中离子浓度大小关系:c(NH4+)=c(Cl-)>c(H+)=c(OH-) |
| C、c点溶液中离子浓度大小关系:c(NH4+)+c(H+)=c(Cl-)+c(OH-) |
| D、d点时溶液温度达到最高,之后温度略有下降,原因是NH3?H2O电离 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com