
| ||
| ||
| ||
| 2×84g×6.2g |
| 62g |
| 33.2g |
| 50g |


科目:高中化学 来源: 题型:
88 22 |
A、一个
| ||
| B、Ra元素位于元素周期表中第六周期ⅡA族 | ||
| C、RaCl2难溶于水 | ||
| D、Ra(OH)2是一种两性氢氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| A、还原剂是浓HCl,氧化剂是MnO2 |
| B、每生成1mol Cl2,转移电子2mol |
| C、每消耗1mol MnO2,浓HCl被还原4mol |
| D、转移1mol电子时,生成的Cl2在标准状况下体积为11.2 L |
查看答案和解析>>
科目:高中化学 来源: 题型:
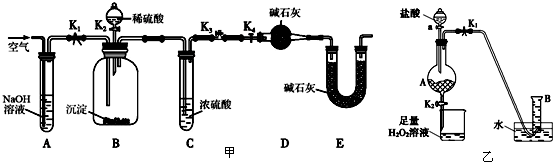
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验步骤(不要求写出具体操作过程) | 预期实验现象和结论 |
| 取少量黑色固体, |
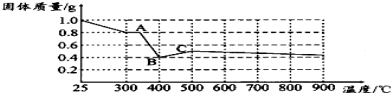
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com