
| A. | NaOH•H2O | B. | NaOH | C. | Na2O2•2H2O | D. | Na2O2•8H2O |
分析 计算过氧化钠物质的量,假设过氧化钠全部反应,根据Na原子守恒计算选项中各物质的质量,质量大于或等于16.8g符合题意.
解答 解:7.8g过氧化钠物质的量为$\frac{7.8g}{78g/mol}$=0.1mol,
假设过氧化钠全部反应,由钠原子守恒:
得到NaOH•H2O为0.2mol,质量为0.2mol×58g/mol=11.6g<16.8g,
得到NaOH为0.2mol,质量为0.2mol×40g/mol=8g<16.8g,
得到Na2O2•2H2O为0.1mol,质量为0.1mol×114g/mol=11.4g<16.8g,
得到Na2O2•8H2O为0.1mol,质量为0.1mol×222g/mol=22.2g>16.8g,
故此固体物质中一定含有Na2O2•8H2O,
故选:D.
点评 本题考查化学计算,侧重考查学生分析计算能力,注意利用验证法解答.


 阶梯计算系列答案
阶梯计算系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 随着人类对温室效应和资源短缺等问题的重视,如何降低大气中CO2的含量及有效地开发利用CO2,引起了各国的普遍重视.
随着人类对温室效应和资源短缺等问题的重视,如何降低大气中CO2的含量及有效地开发利用CO2,引起了各国的普遍重视.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铍原子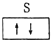 | B. | 碳原子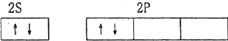 | ||
| C. | 氯原子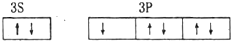 | D. | 铝原子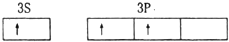 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
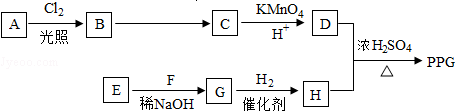
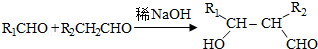
 .
. .
.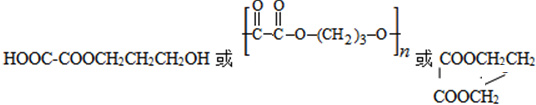 .
.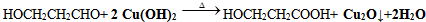 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数 | 1.8×10-5 | K1 4.3×10-7 K2 5.6×10-11 | 3.0×10-8 |
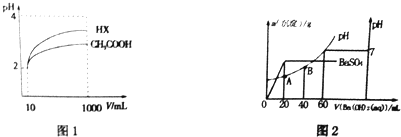
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3-甲基-4-乙基戊烷 | B. | 3,4,4-三甲基己烷 | ||
| C. | 3-甲基-5-己烯 | D. | 3,3-二甲基-1-戊烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2c=b | B. | c=+285.8 | ||
| C. | 通过原电池可以实现反应(3) | D. | 氢气的燃烧热为a kJ/mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com