
| A. | 氨水 | B. | 硝酸 | C. | 酒精 | D. | 醋 |
分析 “强水”“性最烈,能蚀五金…其水甚强,五金八石皆能穿第,惟玻璃可盛.”说明“强水”腐蚀性很强,能腐蚀多数金属及岩石,但不能腐蚀玻璃,即和玻璃中成分不反应,据此分析解答.
解答 解:A.氨水属于弱碱,和金属不反应,不符合条件,故A错误;
B.硝酸具有强氧化性、强酸性,能腐蚀大多数金属,也能和岩石中的CaCO3发生反应,但不能和玻璃中成分硅酸盐反应,所以符合条件,故B正确;
C.酒精是非电解质,不能腐蚀较不活泼金属,如Cu等金属,不符合条件,故C错误;
D.醋其主要成份为醋酸,和大多数金属反应,但无强腐蚀性不符合条件,故D错误;
故选B.
点评 本题考查元素化合物知识,为高频考点,明确物质的性质是解本题关键,知道硝酸的强氧化性,题目难度不大.


 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HCl+Na2CO3;H2SO4+K2CO3 | B. | Fe+HCl;Fe+H2SO4 | ||
| C. | BaCl2+Na2SO4;Ba(OH)2+(NH4)2SO4 | D. | KOH+CH3COONH4;Ba(OH)2+NH4Cl |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
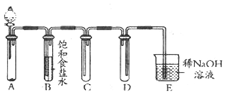 如图是用KMnO4与浓盐酸反应制取适量氯气的简易装置.
如图是用KMnO4与浓盐酸反应制取适量氯气的简易装置.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
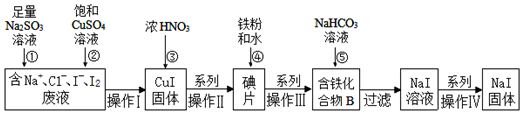
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
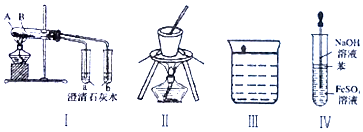
| A. | 图I中A盛放碳酸氢钠,B盛放碳酸钠,可对比二者的热稳定性 | |
| B. | 图II可用于在碳酸钠溶液中提取碳酸钠固体 | |
| C. | 图III为钠与水的反应现象探究实验的装置 | |
| D. | 图 IV为实验室制备观察氢氧化亚铁的装置 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在使石蕊试液变红的溶液中:Na+、K+、Br-、SO42- | |
| B. | 氯化亚铁溶液中:K+、Al3+、SO42-、MnO4- | |
| C. | 硫酸铝溶液中:K+、AlO2-、Na+、Cl- | |
| D. | 与铝反应产生大量氢气的溶液:NH4+、Na+、SO42-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com