
【题目】取一小块金属钠,放在燃烧匙里加热,下列实验现象描述正确的是( )
① 金属先熔化 ② 在空气中燃烧,产生苍白色火焰 ③ 燃烧后得白色固体
④ 燃烧时火焰为黄色 ⑤ 燃烧后生成浅黄色固体物质
A. ② ⑤ B. ①②③ C. ①④⑤ D. ④⑤
 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案科目:高中化学 来源: 题型:
【题目】一定温度下,将足量的AgCl分别放入下列物质中,AgCl的溶解度由大到小的排列顺序是
①20 mL 0.01 mol/L KCl溶液 ②30 mL 0.02 mol/L CaCl2溶液
③40 mL 0.03 mol/L HCl溶液 ④10 mL 蒸馏水⑤50 mL 0.05 mol/L AgNO3溶液
A. ①>②>③>④>⑤ B. ④>①>③>②>⑤
C. ⑤>④>②>①>③ D. ④>③>⑤>②>①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某有机物A的红外光谱和核磁共振氢谱如图所示,下列说法中错误的是( )

A. 由红外光谱可知,该有机物中至少有三种不同的化学键
B. 由核磁共振氢谱可知,该有机物分子中有三种不同化学环境的氢原子
C. 仅由其核磁共振氢谱无法得知其分子中的氢原子总数
D. 若A的化学式为C2H6O,则其结构简式为CH3—O—CH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 被广泛用于食品调味剂,其某种合成路线如下所示。
被广泛用于食品调味剂,其某种合成路线如下所示。
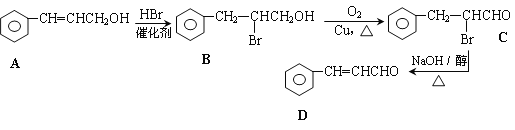
回答如下问题:
(1)B中的官能团名称为_______________
(2)C生成D的反应类型为_____________
(3)在以上路线中,HBr的作用是__________________________________________________
(4) ![]() ,从甲醛、乙醛、丙醛中选择原料(无机原料任选),仿照上述合成路线,写出分两步合成C(CH2OH)4的合成路线_____________________________________________________________
,从甲醛、乙醛、丙醛中选择原料(无机原料任选),仿照上述合成路线,写出分两步合成C(CH2OH)4的合成路线_____________________________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列做法有利于环境保护和可持续发展的是
A. 将工业污水直接用于灌溉农田
B. 将废铅蓄电池的铅泥和废硫酸作深埋处理
C. 推广新能源汽车,建设绿色低碳的交通体系
D. 大力开采煤、石油等化石能源,满足发展需求
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在实验室中可用下图所示装置制取氯酸钾、次氯酸钠和探究氯水的性质。图中:
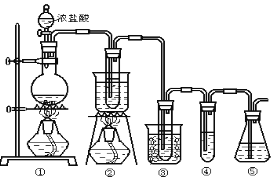
①为氯气发生装置;②的试管里盛有15mL30%KOH溶液,并置于热水浴中;③的试管里盛有15mL8%NaOH溶液,并置于冰水浴中;④的试管里加有紫色石蕊试液;⑤为尾气吸收装置。请填写下列空白:
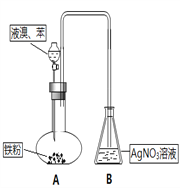
(1)制取氯气时,在烧瓶里加入一定量的二氧化锰,通过_________(填写仪器名称)向烧瓶中加入适量的浓盐酸。实验时为了除去氯气中的氯化氢气体,可在①与②之间安装盛有____________(填写下列编号字母)的净化装置。
A.碱石灰 B.饱和食盐水 C.浓硫酸 D.饱和碳酸氢钠溶液
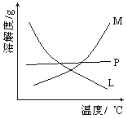
(2)比较制取氯酸钾和次氯酸钠的条件,二者的差异是_____________。反应完毕经冷却后,②的试管中有大量晶体析出。图中符合该晶体溶解度曲线的是_______(填写编号字母);从②的试管中分离出该晶体的方法是_________(填写实验操作名称)。
(3)本实验中制取次氯酸钠的离子方程式是:_______________________。
(4)实验中可观察到④的试管里溶液的颜色发生了如下变化:紫色→______→_______→黄绿色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水中含有丰富的镁资源。某同学设计了从模拟海水中制备MgO的实验方案:
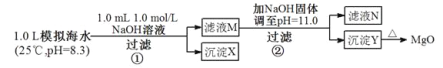
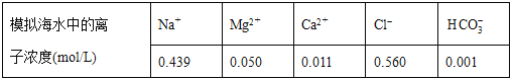
注:溶液中某种离子的浓度小于1.0×10-5mol/L,可认为该离子不存在;实验过程中,假设溶液体积不变。
已知:Ksp(CaCO3)=4.96×10-9;Ksp(MgCO3)=6.82×10-6;Ksp[Ca(OH)2]=4.68×10-6;Ksp[Mg(OH)2]=5.61×10-12。下列说法正确的是( )
A. 沉淀物X为CaCO3
B. 滤液M中存在Mg2+,不存在Ca2+
C. 滤液N中存在Mg2+,Ca2+
D. 步骤②中若改为加入4.2 g NaOH固体,沉淀物Y为Ca(OH)2和Mg(OH)2的混合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组用铁泥(主要成分为Fe2O3、FeO和少量Fe)制备Fe3O4纳米材料的流程示意图如下:


已知:步骤⑤中,相同条件下测得Fe3O4的产率与R( )的关系如图所示。
)的关系如图所示。
(1)为提高步骤①的反应速率,可采取的措施是_______________(任写一点) 。
(2)步骤②中,主要反应的离子方程式是________________________。
(3)浊液D中铁元素以FeOOH形式存在。步骤④中,反应的化学方程式是___________________;步骤④中,反应完成后需再加热一段时间除去剩余H2O2目的是____________________________
(4)⑤反应的离子方程式为_________________ ;步骤⑤中的“分离”包含的步骤有______________________。
(5)设浊液D中FeOOH的物质的量为amol,滤液B中的铁元素的物质的量为bmol。为使Fe3O4的产率最高,则![]() =_________。(填数值,小数点后保留3位)
=_________。(填数值,小数点后保留3位)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com