
| A. | 35Cl原子所含质子数为18 | |
| B. | $\frac{1}{18}$ mol的H35Cl分子所含中子数约为6.02×1023 | |
| C. | 3.5 g的35Cl2气体的体积为2.24 L | |
| D. | 35Cl2气体的摩尔质量为70 |
分析 A、35Cl是氯的一种同位素,质子数等于原子序数.
B、根据质量数=质子数+中子数计算分子中各原子的中子数,计算出1个分子含有的中子数,再根据N=nNA计算.
C、不一定处于标准状况,不能使用气体摩尔体积22.4L/mol.
D、摩尔质量的单位是g/mol.
解答 解:A、35Cl是氯的一种同位素,质子数等于原子序数,所以35Cl质子数为17,故A错误;
B、H35Cl分子所含中子为18,$\frac{1}{18}$mol的H35Cl分子所含中子的物质的量为1mol,所以中子数约为6.02×1023,故B正确;
C、氯气不一定处于标准状况,不能使用气体摩尔体积22.4L/mol,故C错误;
D、35Cl2气体的摩尔质量为70g/mol,故D错误;
故选B.
点评 本题考查原子符号、物质的量的有关计算、摩尔质量、气体摩尔体积等,注意气体摩尔体积使用条件与范围,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 单位时间内形成x mol的A-A键,同时形成x mol的A-B键 | |
| B. | 容器内的总压强不随时间变化,气体的密度不再随时间变化 | |
| C. | A2、AB、B2的浓度不再随时间改变 | |
| D. | 单位时间内生成x mol的A2分子,同时生成x mol的B2分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 由短周期元素组成的甲、乙和丙均为中学常见物质,一定条件下,存在转化关系:甲$\stackrel{强酸溶液}{←}$丙$\stackrel{强碱溶液}{→}$乙
由短周期元素组成的甲、乙和丙均为中学常见物质,一定条件下,存在转化关系:甲$\stackrel{强酸溶液}{←}$丙$\stackrel{强碱溶液}{→}$乙查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 锂、钠、钾、铷、铯都具有碱性,故称为碱金属 | |
| B. | 石灰石、纯碱、小苏打、碳酸铵热稳定性最强的是纯碱 | |
| C. | 过氧化钠投入到饱和碳酸钠溶液既能产生白色沉淀,又能产生气体 | |
| D. | 金属Li是密度最小的碱金属,熔点大于Rb |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

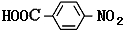 .
.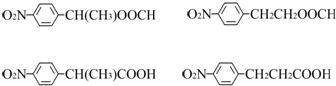 任意2种.
任意2种.
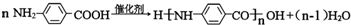 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NO2、SO2、BF3、NCl3分子中各原子均不满足最外层8电子结构 | |
| B. | 某化合物的焰色反应为黄色,则该化合物一定为钠盐 | |
| C. | NaCl晶体中与每个Na+距离相等且最近的Na+共有6个 | |
| D. | 单质的晶体中一定不存在的微粒是阴离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电解精炼铜的过程中,若阳极有64g铜放电溶解,则理论上电路中转移的电子数为2NA | |
| B. | 7.8g Na2O2与Na2S的混合物中含有的阴、阳离子的总数为0.3NA | |
| C. | 0.1 mol/LNa2CO3溶液中所含阴离子的总数大于0.1NA | |
| D. | 标准状况下22.4L三氯甲烷含有氯原子的数目是3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫酸亚铁在空气中被氧化:4Fe2++3O2+6H2O═4Fe(OH)3 | |
| B. | 向CH2Br-COOH中加入足量的NaOH溶液并加热:CH2Br-COOH+OH-$\stackrel{△}{→}$CH2Br-COO-+H2O | |
| C. | FeCl3溶液中通入SO2,溶液黄色褪去:2Fe3++SO2+2H2O═2Fe2++SO42-+4H+ | |
| D. | 碳酸钠溶液滴入酚酞变红:CO32-+2H2O?H2CO3+2OH- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com