
����Ŀ�����������һ�����Ϳɳ���أ�����ͨ���ܵ����ȣ��õ�س�ʱ�䱣���ȶ��ķŵ��ѹ��������ص��ܷ�ӦΪ3Zn��2K2FeO4��8H2O![]() 3Zn(OH)2��2Fe(OH)3��4KOH��������������ȷ����
3Zn(OH)2��2Fe(OH)3��4KOH��������������ȷ����
A.�ŵ�ʱ������ӦΪ��Zn��2OH����2e����Zn(OH)2
B.���ʱ������ӦΪ��Fe(OH)3��5OH����3e����FeO42����4H2O
C.�ŵ�ʱÿת��3mol���ӣ�������1mol K2FeO4������
D.�ŵ�ʱ����������Һ�ļ�����ǿ
���𰸡�C
��������
A��ŵ�ʱ��Zn����������������Zn��OH��2���缫��ӦʽΪ3Zn-6e-+6OH-�T3Zn��OH��2����A��ȷ��
B����ʱ��Fe(OH)3����������������Ӧ����FeO42�����缫��ӦʽΪFe(OH)3��5OH����3e����FeO42����4H2O����B��ȷ��
C��ŵ�ʱ��Fe���ϼ���+6�۽���Ϊ+3�ۣ���ŵ�ʱÿת��3mol���ӣ�������1molK2FeO4����ԭ����C����
D��ŵ�ʱ��K2FeO4Ϊ��ص��������õ��ӷ�����ԭ��Ӧ����Fe��OH��3���缫��ӦʽΪ2FeO42-+6e-+8H2O�T2Fe��OH��3+10OH-����������OH-����Һ������ǿ����D��ȷ��
��ѡC��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ֲ�ͬ�ѻ���ʽ�Ľ�������ľ�����ͼ��ʾ���й�˵����ȷ����
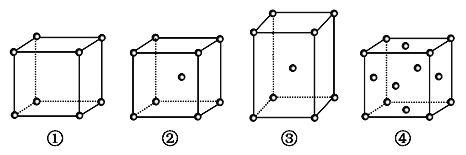
A.������ԭ�ӵ���λ���ֱ�Ϊ��6����8����8����12
B.�ռ������ʵĴ�С��ϵΪ��<��<��<��
C.��Ϊ�������ѻ�����Ϊþ�ͣ���Ϊ���ͣ���Ϊͭ��
D.ÿ���������е�ԭ�����ֱ�Ϊ��1������2������2������4��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ�������£���3molA��1molBͶ���ݻ�Ϊ2L���ܱ������У��������·�Ӧ��3A��g��+B��g��![]() xC��g��+2D��g����2minĩ��ô�ʱ������C��D��Ũ��Ϊ0.2mol/L��0.4mol/L������������ȷ���� �� ��
xC��g��+2D��g����2minĩ��ô�ʱ������C��D��Ũ��Ϊ0.2mol/L��0.4mol/L������������ȷ���� �� ��
A. x=2
B. 2minʱ��B��Ũ��Ϊ0.4mol/L
C. 0��2min��B�ķ�Ӧ����Ϊ0.2mol��L����min��
D. ��ʱA��ת����Ϊ40��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��X��Y��Z��W����������һ�������¾�����ͼ��ʾ��ת����ϵ![]() ����������ȥ
����������ȥ![]() ��
��
![]()
�����ж���ȷ����![]()
A.��ͼ�з�Ӧ��Ϊ��������ԭ��Ӧ��WΪ![]() ����X������
����X������![]()
B.��ͼ�з�Ӧ��Ϊ������ԭ��Ӧ��WΪ![]() ����Z������
����Z������![]()
C.��ͼ�з�Ӧ��Ϊ��������ԭ��Ӧ��WΪNaOH����Y������![]()
D.��ͼ�з�Ӧ��Ϊ������ԭ��Ӧ��WΪ![]() ����X������
����X������![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ڷ�ӦA2(g)��3B2(g)![]() 2AB3(g)��˵�����з�Ӧ�����б�ʾ�÷�Ӧ���е������ǣ� ��
2AB3(g)��˵�����з�Ӧ�����б�ʾ�÷�Ӧ���е������ǣ� ��
A.v(AB3)��12mol��L��1��min��1B.v(B2)��2.7mol��L��1��min��1
C.v(A2)��0.25mol��L��1��s��1D.v(A2)��6mol��L��1��min��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���״����ӽ���Ĥȼ�ϵ���н��״�����ת��Ϊ���������ַ�Ӧԭ���緽��ʽ�٢���ʾ��
��CH3OH(g)+H2O(g)=CO2(g)+3H2(g)�� ��H=+49.0kJmol-1
��CH3OH(g)+![]() O2(g)=CO2(g)+2H2(g)����H=-192.9kJmol-1
O2(g)=CO2(g)+2H2(g)����H=-192.9kJmol-1
��H2(g)+![]() O2(g)=H2O(g)����H=-241.8kJmol-1
O2(g)=H2O(g)����H=-241.8kJmol-1
����˵����ȷ���ǣ� ��
A.CH3OH��ȼ����Ϊ192.9kJmol-1
B.��Ӧ���е������仯��ͼ��ʾ
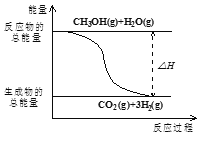
C.CH3OHת���H2�Ĺ���һ��Ҫ��������
D.�������Ϸ�Ӧ��֪��CH3OH(g)+![]() O2(g)=CO2(g)+2H2O(g)����H=-676.5kJmol-1
O2(g)=CO2(g)+2H2O(g)����H=-676.5kJmol-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���淴Ӧ��2A(g)��3B(g) ![]() xC(g)��4D(g)�������������������ͬ��ͬ������ܱ������н��з�Ӧ����0.8 mol A��1.2 mol B��1.2 mol C��2.4 mol D��1.4 mol A��2.1 mol B��0.6 mol C��1.2 mol D��ƽ���C������������ȣ���ʽ��x��ֵΪ( )
xC(g)��4D(g)�������������������ͬ��ͬ������ܱ������н��з�Ӧ����0.8 mol A��1.2 mol B��1.2 mol C��2.4 mol D��1.4 mol A��2.1 mol B��0.6 mol C��1.2 mol D��ƽ���C������������ȣ���ʽ��x��ֵΪ( )
A. 1B. 2C. 3D. 4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ڷ�Ӧ��2A(g)��B(g)![]() 2C(g) ��H��0������ͼ����ȷ���ǣ� ��
2C(g) ��H��0������ͼ����ȷ���ǣ� ��
A.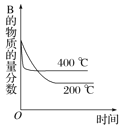 B.
B.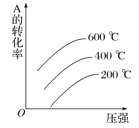
C.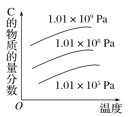 D.
D.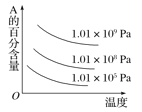
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ƥ��J(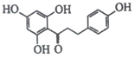 )�ǹ����½��о�����������һ��������Ȼ����,��Ҫ�ֲ���ƻ������ȶ�֭ˮ���Ĺ�Ƥ����Ƥ.����һ�ֺϳ�J��·�����£�
)�ǹ����½��о�����������һ��������Ȼ����,��Ҫ�ֲ���ƻ������ȶ�֭ˮ���Ĺ�Ƥ����Ƥ.����һ�ֺϳ�J��·�����£�
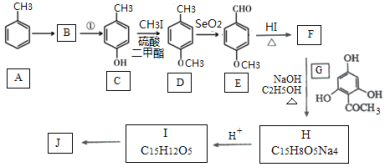
��֪��
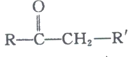 +R����CHO
+R����CHO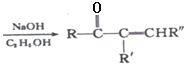 +H2O
+H2O
�ش��������⣺
(1)C�Ļ�ѧ������___________.E�еĹ����ŵ�����Ϊ_______________.
(2)BΪ�����,��д��A��B�ķ�Ӧ����___________.
(3)д����C����D����D����E�ķ�Ӧ����___________��___________.
(4)F��H�Ļ�ѧ����ʽΪ______________________.
(5)M��E��ͬ���칹��,ͬʱ��������������M�Ľṹ��___________��(�����������칹)
������FeCl3��Һ������ɫ��Ӧ ���ܷ���������Ӧ
(6)����Ա�ϩ��1,3������ȩΪ��ʼԭ���Ʊ�![]() �ĺϳ�·��_______(���Լ���ѡ).
�ĺϳ�·��_______(���Լ���ѡ).
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com