
在室温下,将铁片、铜片、铝片(表面用砂纸打磨过)分别投入浓盐酸、浓硫酸、浓硝酸、浓氢氧化钠溶液中,做了12个实验,实验的编号如下表所示.
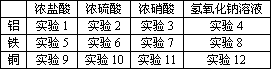
回答有关这12个实验的下列问题:(下列空格中填写的实验编号可能不止一个)
(1)三种金属投入以上一种试剂中均无明显现象,这种试剂是________.
(2)若给以上溶液加热,也不会发生化学反应的实验是________(填实验编号).
(3)能比较三种金属的金属性强弱的实验是________(填实验编号).
(4)有一个实验最能直观证明硝酸具有强氧化性,该实验的编号是________;该实验中1 mol HNO3参加反应,氧化这种金属________mol.
(5)以上发生的化学反应中,有一种溶液中的溶质并没有起氧化剂的作用,该实验的编号为________,该实验中1 mol金属还原________摩氧化剂.
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:导学大课堂必修一化学人教版 人教版 题型:043
如果在室温时试验铁片在硝酸中的反应速率与硝酸浓度的关系,我们将会发现铁的反应速率最初是随硝酸浓度的增大而增大.当增大到一定程度时,它的反应速率迅速减小,继续增大硝酸的浓度时,它的反应速率更小,最后不再起反应,即铁变得“稳定”了.
这种现象叫金属的“钝化”,是由于浓硝酸具有强氧化性,在铁的表面氧化生成了一层致密的氧化物薄膜,隔离了内部的金属与浓硝酸的接触,使反应自动终止.
不仅铁,其他一些金属也可以发生钝化.例如,Cr、Ni、Co、Mo、Al、Ta、Nb和W等,其中最容易钝化的金属是Cr、Mo、Al、Ni、Fe.
不仅硝酸,其他强氧化剂如浓硫酸、氯酸、碘酸、重铬酸钾、高锰酸钾等,都可以引起金属的钝化.
在个别情况下,少数钨能在非氧化剂介质中钝化.例如,镁在HF中钝化,钼和铌在HCl中钝化.
一般的说,钝化后的金属,在改变外界钝化条件后,仍能在相当程度上保持钝化状态.例如,铁在浓硝酸中钝化后,不仅在稀硝酸中保持稳定,而且在水、水蒸气及其他介质中也能保持稳定.钝化后的铁不能从硝酸铜溶液中置换出铜.
使金属钝化的方法,除了把金属浸在浓酸里使它钝化外,还可以把金属作为电极(阳极),通过电流使它发生氧化.当电流密度增大到一定程度时,金属就能被钝化.
问题:金属的钝化,使之变得“稳定”,那么能不能破坏这种钝化状态呢?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com