
�����£���0.05 mol Na2CO3��������ˮ���100mL��Һ������Һ�м����������ʡ��йؽ�����ȷ���ǣ� ��
| ��������� | ���� | |
| A | 50mL 1 mol��L��1H2SO4 | ��Ӧ������c(Na+)=c(SO42��) |
| B | 0.05molCaO | ��Һ�� |
| C | 50mL H2O | ��ˮ�������c(H+)��c(OH��)���� |
| D | 0.1molNaHSO4���� | ��Ӧ��ȫ����ҺpH��С��c(Na+)���� |
���𰸡�B
�������������£���0.05 mol Na2CO3��������ˮ���100mL��Һ����Һ�д���CO32��+H2O HCO3��+OH����Һ�ʼ��ԣ�A�����50mL 1 mol��L��1H2SO4��H2SO4��Na2CO3ǡ�÷�Ӧ����Ӧ�����Һ����ΪNa2SO4���ʸ��������غ㷴Ӧ������c(Na+)=2c(SO42��)����A���������Һ�м���0.05molCaO����CaO+ H2O=Ca(OH)2����c(OH��)������Ca2++CO32��=CaCO3����ʹCO32��+H2O
HCO3��+OH����Һ�ʼ��ԣ�A�����50mL 1 mol��L��1H2SO4��H2SO4��Na2CO3ǡ�÷�Ӧ����Ӧ�����Һ����ΪNa2SO4���ʸ��������غ㷴Ӧ������c(Na+)=2c(SO42��)����A���������Һ�м���0.05molCaO����CaO+ H2O=Ca(OH)2����c(OH��)������Ca2++CO32��=CaCO3����ʹCO32��+H2O HCO3��+OH��ƽ�����ƣ�c(HCO3��)��С����
HCO3��+OH��ƽ�����ƣ�c(HCO3��)��С����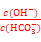 ����B����ȷ��C�����50mL H2O����Һ������CO32��+H2O
����B����ȷ��C�����50mL H2O����Һ������CO32��+H2O HCO3��+OH��ƽ�����ƣ���c(OH��)��С��Na2CO3��Һ��H+��OH������ˮ���룬����ˮ�������c(H+)��c(OH��)��С����C�����D�����0.1molNaHSO4���壬NaHSO4Ϊǿ����ʽ�ε����H+��CO32����Ӧ����Ӧ����ҺΪNa2SO4��Һ����Һ�����ԣ�����ҺpH��С��������Na+����c(Na+)����D�������ѡB��
HCO3��+OH��ƽ�����ƣ���c(OH��)��С��Na2CO3��Һ��H+��OH������ˮ���룬����ˮ�������c(H+)��c(OH��)��С����C�����D�����0.1molNaHSO4���壬NaHSO4Ϊǿ����ʽ�ε����H+��CO32����Ӧ����Ӧ����ҺΪNa2SO4��Һ����Һ�����ԣ�����ҺpH��С��������Na+����c(Na+)����D�������ѡB��
�����㶨λ��������Ҫ����������ˮ��ƽ��Ӧ�á��漰����Ũ�ȵıȽϡ���ֵ�ı仯����ҺpH�ı仯��
����ʦ�㾦���ε�ˮ����������ݺܶ࣬������Һ������Ũ�ȵı仯��ˮ�����ӻ��ı仯������ƽ�ⳣ����ˮ��ƽ�ⳣ������ҺpH���жϡ�ˮ�����ӷ���ʽ����д����ˮ���Ӧ�á�����غ���ɡ������غ���ɡ������غ���ɵ�Ӧ�ã����������Լ���ˮ��ƽ���Ӱ�졢ϡ���ɵȣ�������Ŀץסˮ��Ҳ�ǿ��淴Ӧ�����Կ�Ӧ����������ԭ������𡣶��������ĸı���Һ������Ũ�ȵı仯�������ж�ƽ���ƶ��Ļ����Ͻ����жϣ���ʱ����ƽ�ⳣ�����غ���ɵȣ������ǵ�ʽ��ϵ������Ũ�ȵ��жϻ�����Ũ�ȴ�С�Ƚ��DZ�֪ʶ���ѵ㡣��ʽ��ϵ��һ������غ�������������ʽ��ֻ�������ӣ�һ��Ҫ���ǵ���غ㣻��ʽ�������ӡ����Ӿ����ڣ�һ�㿼�������غ�������غ㣻����Ũ�ȵıȽ�Ҫ������Һ������ԡ�ˮ�⡢����̶ȵ����ǿ���Ĺ�ϵ��


 ���ɶ���ܲ��¿�ֱͨ�п�ϵ�д�
���ɶ���ܲ��¿�ֱͨ�п�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
Ԫ��X��Y��Zԭ������֮��Ϊ37��X��Y��ͬһ���ڣ�X����Z��������ͬ�ĺ�����Ӳ�ṹ�������Ʋⲻ��ȷ����(����)
A��ͬ��Ԫ����Z���⻯���ȶ������
B��ͬ����Ԫ����X�Ľ�������ǿ
C��ԭ�Ӱ뾶X>Y�����Ӱ뾶X��>Z��
D��ͬ����Ԫ����Y����ۺ������������ǿ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ȩ���Ը����������Ƶı�����Һ�����ӳɷ�Ӧ������ ����ˮ���Ե����ǻ������ƣ�
����ˮ���Ե����ǻ������ƣ�

��Ӧ �ǿ���ģ���ͨ����������70%��90%������Ӧ����ת����
�ǿ���ģ���ͨ����������70%��90%������Ӧ����ת����
(1)���屽�л������ʱ���ȩ������������ȫ����ȥ���ɲ��õ��Լ���__________________������뷽��Ϊ__________________��
(2)����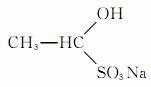 ˮ��Һ�м����������ᣬ�л���ת��Ϊ________������ת�������������ij��÷�����________��
ˮ��Һ�м����������ᣬ�л���ת��Ϊ________������ת�������������ij��÷�����________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���й��ڻ�ѧʵ���������ȷ����
A���ú�ɫʯ����ֽ����NH3����pH��ֽ����Һ��pH��������������ˮ��ʪ��ֽ
B����Һ©��������ƿ��ʹ��ǰ�������Ƿ�©ˮ
C�����ˡ�����������0.1mol/LNaCl��Һ��������ʹ���ձ��Ͳ�����
D��ʵ����������ˮ������ˮ��ʯ�ͷ�������ϩ��������ʹ���¶ȼ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
I����������(ClO2)�ǹ�����ϵĸ�Ч�����ס����١���ȫ����ɱ��������������Ϊ����4������������
��1����ҵ�ϲ����������Ʊ�ClO2��2NaClO3+4HCl=2ClO2��+Cl2��+2H2O+2NaCl��
��Ũ�����ڷ�Ӧ����ʾ������������ ������ĸ��ţ���
A.ֻ�л�ԭ�� B.��ԭ�Ժ����� C.ֻ�������� D.�����Ժ�����
�ڵ�����0.4molClO2ʱ��ת�Ƶ��� mol��
��������˫��ˮ��ԭ�������Ʊ�ClO2�����ʺ���������ˮ������������Ҫԭ���� ��
��2��ClO2��ɱ��������ͬʱ���ɽ��綾�軯�����������������ȥ��д����ClO2
������ȥCN�������ӷ���ʽ ��
II����ͼ������H2��ԭ CO2�Ʊ��״���ԭ��ع���ԭ��ʾ��ͼ��ͼ������ͼ������Դʵ��CO2�Ʊ�̼�⻯��Ĺ���ԭ��ʾ��ͼ����KHSO4��Һ�����Һ����
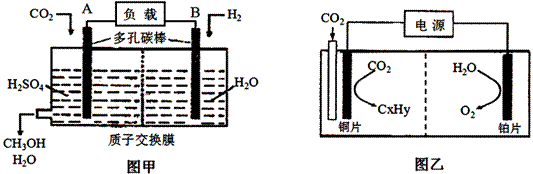
��1��ͼ����A�ĵ缫������ ��
��2��������̼�⻯��ΪC2H4�� ��ͭ�缫�ĵ缫��ӦΪ ��
��3����ͨ���CO2ȫ���μӷ�Ӧ�������й�����0.6molCO2 ʱ��ͼ����ͨ�����ӽ���Ĥ��H+ �����ʵ���Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ȷ��ȡ20.00mLij����HCl��Һ����ƿ�У���0.1000mol��L-1NaOH��Һ�ζ�������˵����ȷ���ǣ� ��
A���ζ���������ˮϴ�Ӻ�װ��NaOH��Һ���еζ�
B������NaOH��Һ���룬��ƿ����ҺpH��С���
C���÷�̪��ָʾ��������ƿ����Һ�ɺ�ɫ����ɫʱֹͣ�ζ�
D���ζ����յ�ʱ�����ֵζ��ܼ��첿�������Σ���ⶨ���ƫС
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���Ǻϳ����ᡢ狀͵��ʵĻ���ԭ�ϣ��ش��������⣺
��1������ˮ��Һ�������ԣ���ԭ��Ϊ �������ӷ���ʽ��ʾ����0��1 mol��L-1�İ�ˮ�м���������NH4Cl���壬��Һ��PH ������ߡ����͡�������������������������Һ�е�NH4+��Ũ�� �������С������
 ��2������識��ȷֽ�ɵõ�N2O��H2O��250��ʱ����������ܱ������зֽ�ﵽƽ�⣬�÷ֽⷴӦ�Ļ�ѧ����ʽΪ ��ƽ�ⳣ������ʽΪ ������1mol�������ȫ�ֽ⣬ת�Ƶĵ�����Ϊ mol��
��2������識��ȷֽ�ɵõ�N2O��H2O��250��ʱ����������ܱ������зֽ�ﵽƽ�⣬�÷ֽⷴӦ�Ļ�ѧ����ʽΪ ��ƽ�ⳣ������ʽΪ ������1mol�������ȫ�ֽ⣬ת�Ƶĵ�����Ϊ mol��
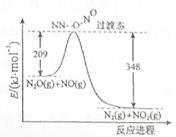
��3����N2O��NO��Ӧ����N2��NO2�������仯��ͼ��ʾ��������1molN2�� ���H= kJ��mol-1��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��O2��HClת��ΪCl2�������Ч�棬������Ⱦ��
��1����ͳ�ϸ�ת��ͨ������ͼ��ʾ�Ĵ���ѭ��ʵ�֣�

���У���Ӧ��Ϊ��2HCl(g) + CuO(s)  H2O(g)+CuCl2(g) ��H1
H2O(g)+CuCl2(g) ��H1
��Ӧ������1molCl2(g)�ķ�Ӧ��Ϊ��H2�����ܷ�Ӧ���Ȼ�ѧ����ʽΪ , (��Ӧ���á�H1�͡�H2��ʾ)��
��2������RuO2����������HClת��ΪCl2���ܷ�Ӧ���и��õĴ����ԣ�
��ʵ������һ��ѹǿ�£��ܷ�Ӧ��HClƽ��ת�������¶ȱ仯��aHCl��T������ͼ12�����ܷ�Ӧ�ġ�H 0 ,�����������������������A��B�����ƽ�ⳣ��K(A)��K(B)�нϴ���� ��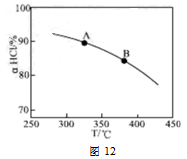
��������ʵ������ѹ�����ʹѹǿ��������ӦaHCl��T���ߵ�ʾ��ͼ������Ҫ˵�����ɣ� ��
�����д�ʩ�����������aHCl����  ��
��
A������n(HCl) B������n(O2) C��ʹ�ø��õĴ��� D����ȥH2O
��3��һ�������²�÷�Ӧ������n(Cl2)���������£�
| t(min) | 0 | 2.0 | 4.0 | 6.0 | 8.0 |
| n(Cl2)/10-3mol | 0 | 1.8 | 3.7 | 5.4 | 7.2 |
����2.0��6.0min����HCl�����ʵ����仯��ʾ�ķ�Ӧ���ʣ���mol��min-1Ϊ��λ��д��������̣���
��4��Cl2��;�㷺��д����Cl2�Ʊ�Ư�۵Ļ�ѧ����ʽ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���жԻ�ѧ��Ӧ�������˵����ȷ����(����)
A�����ȷ�Ӧ����ʱ���ؼ���
B����ѧ��Ӧһ���������仯
C��һ���˵�����ȷ�Ӧ���Ⱥ���ܷ���
D����ѧ��Ӧ����ЧӦ��ֵ��μӷ�Ӧ�����ʵĶ�����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com