
”¾ĢāÄæ”æ¼×“¼ŹĒÖŲŅŖµÄ»Æѧ¹¤Ņµ»ł“”ŌĮĻŗĶĒå½ąŅŗĢåČ¼ĮĻ£®¹¤ŅµÉĻæÉĄūÓĆCO»ņCO2Ą“Éś²śČ¼ĮĻ¼×“¼£®ŅŃÖŖÖʱø¼×“¼µÄÓŠ¹Ų»Æѧ·“Ó¦ŅŌ¼°ŌŚ²»Ķ¬ĪĀ¶ČĻĀµÄ»ÆŃ§Ę½ŗā³£ŹżČē±ķĖłŹ¾£ŗ
»Æѧ·“Ó¦ | Ę½ŗā³£ĪĀ | ĪĀ¶Č£Ø”ę£© | |
500 | 800 | ||
¢Ł2H2£Øg£©+CO£Øg£©CH3OH£Øg£© | K1 | 2.5 | 0.15 |
¢ŚH2£Øg£©+CO2£Øg£©H2O£Øg£©+CO£Øg£© | K2 | 1.0 | 2.5 |
¢Ū3H2£Øg£©+CO2£Øg£©CH3OH£Øg£©+H2O£Øg£© | K3 | ||
£Ø1£©·“Ó¦¢ŚŹĒ£ØĢī”°ĪüČČ”±»ņ”°·ÅČČ”±£©·“Ó¦£®
£Ø2£©Ä³ĪĀ¶ČĻĀ·“Ó¦¢ŁÖŠH2µÄĘ½ŗā×Ŗ»ÆĀŹ£Øa£©ÓėĢåĻµ×ÜŃ¹Ēæ£Øp£©µÄ¹ŲĻµČēĶ¼¼×ĖłŹ¾£®ŌņĘ½ŗāדĢ¬ÓÉA±äµ½BŹ±£¬Ę½ŗā³£ŹżK£ØA£©K£ØB£©£ØĢī”°£¾”±”°£¼”±»ņ”°=”±£©£® 
£Ø3£©¾Ż·“Ó¦¢ŁÓė¢ŚæÉĶʵ¼³öK1”¢K2ÓėK3Ö®¼äµÄ¹ŲĻµ£¬ŌņK3=£ØÓĆK1”¢K2±ķŹ¾£©£®500”ꏱ²āµĆ·“Ó¦¢ŪŌŚÄ³Ź±æĢŹ±£¬H2£Øg£©”¢CO2£Øg£©”¢CH3OH£Øg£©”¢H2O£Øg£©µÄÅØ¶Č£ØmolL©1£©·Ö±šĪŖ0.8”¢0.1”¢0.3”¢0.15£¬Ōņ“ĖŹ±vÕżvÄę£ØĢī”°£¾”±”°=”±»ņ”°£¼”±£©£®
£Ø4£©ŌŚ3LČŻ»żæɱäµÄĆܱÕČŻĘ÷ÖŠ·¢Éś·“Ó¦¢Ś£¬ŅŃÖŖc£ØCO£©©t£Ø·“Ó¦Ź±¼ä£©±ä»ÆĒśĻߢńČēĶ¼ŅŅĖłŹ¾£¬ČōŌŚt0Ź±æĢ·Ö±šøıäŅ»øöĢõ¼ž£¬ĒśĻߢń±äĪŖĒśĻߢņŗĶĒśĻߢó
µ±ĒśĻߢń±äĪŖĒśĻߢņŹ±£¬øıäµÄĢõ¼žŹĒ
µ±ĒśĻߢń±äĪŖĒśĻß¢óŹ±£¬øıäµÄĢõŹĒ £® 
”¾“š°ø”æ
£Ø1£©ĪüČČ
£Ø2£©=
£Ø3£©K1?K2£»£¾
£Ø4£©¼ÓČė“߻ƼĮ£»½«ČŻĘ÷µÄĢå»żæģĖŁŃ¹ĖõÖĮ2L
”¾½āĪö”æ½ā£ŗ£Ø1£©·ÖĪöĶ¼±ķŹż¾Ż£¬·“Ó¦¢ŚĘ½ŗā³£ŹżĖęĪĀ¶ČÉżøßŌö“ó£¬Ę½ŗāÕżĻņ½ųŠŠ£¬Õż·“Ó¦ŹĒĪüČČ·“Ó¦£¬ĖłŅŌ“š°øŹĒ£ŗĪüČČ£»£Ø2£©ŅĄ¾ŻĘ½ŗā³£ŹżĖęĪĀ¶Č±ä»Æ£¬²»ĖęŃ¹Ēæ±ä»Æ·ÖĪö£¬Ķ¼ĻóÖŠĘ½ŗāדĢ¬ÓÉA±äµ½BŹ±£¬Ń¹Ēæøı䣬ĪĀ¶Č²»±ä£¬ĖłŅŌĘ½ŗā³£Źż²»±ä£»ĖłŅŌ“š°øŹĒ£ŗ=£»£Ø3£©·“Ó¦¢Ū3H2£Øg£©+CO2£Øg£©ØTCH3OH£Øg£©+H2O£Øg£©ŹĒĘųĢåĢå»ż¼õŠ”µÄ·“Ó¦”÷S£¼0£¬ŅĄ¾Ż·“Ó¦¢Ł+¢ŚµĆµ½·“Ó¦¢Ū£¬ĖłŅŌĘ½ŗā³£ŹżK3=K1”ĮK2£»ŌŚ500”ę”¢2LµÄĆܱÕČŻĘ÷ÖŠ£¬½ųŠŠ·“Ó¦¢Ū£¬²āµĆ·“Ó¦¢ŪŌŚÄ³Ź±æĢ£¬H2£Øg£©”¢CO2£Øg£©”¢CH3OH£Øg£©”¢H2O £Øg£©µÄÅØ¶Č£Ømol/L£©·Ö±šĪŖ0.8”¢0.1”¢0.3”¢0.15£¬Q= ![]() =0.87£¼K=2.5£¬·“Ó¦ÕżĻņ½ųŠŠ£¬VÕż£¾VÄę £¬ ĖłŅŌ“š°øŹĒ£ŗ=£»K1K2£»£¾£»£Ø4£©Ķ¼Ļó·ÖĪöĒśĻߢń±ä»ÆĪŖĒśĻߢņŹĒĖõ¶Ģ·“Ó¦“ļµ½Ę½ŗāµÄŹ±¼ä£¬×īŗó“ļµ½ĻąĶ¬Ę½ŗāדĢ¬£¬Ģå»żŹĒæɱäµĆŹĒŗćŃ¹ČŻĘ÷£¬ĖµĆ÷øıäµÄŹĒ¼ÓČėĮĖ“߻ƼĮ£»µ±ĒśĻߢń±äĪŖĒśĻߢóŹ±Ņ»Ńõ»ÆĢ¼ĪļÖŹµÄĮæŌö“󣬷“Ó¦ŹĒĘųĢåĢå»ż²»±äµÄ·“Ó¦£¬æɱäČŻĘ÷ÖŠĘųĢåĢå»żŗĶÅØ¶Č³É·“±Č£¬ĘųĢåĪļÖŹµÄĮæ²»±ä£¬ĒśĻߢń£¬Ģå»żĪŖ3L£¬Ņ»Ńõ»ÆĢ¼ÅضČĪŖ3mol/L£¬øıäĢõ¼ž²»ŗĆĪŖĒśĻߢņ£¬Ņ»Ńõ»ÆĢ¼ÅضČĪŖ4.5mol/L£¬ŌņĢå»żŃ¹ĖõĢå»żĪŖ£ŗ3£ŗV=4.5£ŗ3£¬V=2L£¬ĖłŅŌ½«ČŻĘ÷µÄĢå»żæģĖŁŃ¹ĖõÖĮ2L·ūŗĻ£»ĖłŅŌ“š°øŹĒ£ŗ¼ÓČė“߻ƼĮ£»½«ČŻĘ÷µÄĢå»żæģĖŁŃ¹ĖõÖĮ2L£®
=0.87£¼K=2.5£¬·“Ó¦ÕżĻņ½ųŠŠ£¬VÕż£¾VÄę £¬ ĖłŅŌ“š°øŹĒ£ŗ=£»K1K2£»£¾£»£Ø4£©Ķ¼Ļó·ÖĪöĒśĻߢń±ä»ÆĪŖĒśĻߢņŹĒĖõ¶Ģ·“Ó¦“ļµ½Ę½ŗāµÄŹ±¼ä£¬×īŗó“ļµ½ĻąĶ¬Ę½ŗāדĢ¬£¬Ģå»żŹĒæɱäµĆŹĒŗćŃ¹ČŻĘ÷£¬ĖµĆ÷øıäµÄŹĒ¼ÓČėĮĖ“߻ƼĮ£»µ±ĒśĻߢń±äĪŖĒśĻߢóŹ±Ņ»Ńõ»ÆĢ¼ĪļÖŹµÄĮæŌö“󣬷“Ó¦ŹĒĘųĢåĢå»ż²»±äµÄ·“Ó¦£¬æɱäČŻĘ÷ÖŠĘųĢåĢå»żŗĶÅØ¶Č³É·“±Č£¬ĘųĢåĪļÖŹµÄĮæ²»±ä£¬ĒśĻߢń£¬Ģå»żĪŖ3L£¬Ņ»Ńõ»ÆĢ¼ÅضČĪŖ3mol/L£¬øıäĢõ¼ž²»ŗĆĪŖĒśĻߢņ£¬Ņ»Ńõ»ÆĢ¼ÅضČĪŖ4.5mol/L£¬ŌņĢå»żŃ¹ĖõĢå»żĪŖ£ŗ3£ŗV=4.5£ŗ3£¬V=2L£¬ĖłŅŌ½«ČŻĘ÷µÄĢå»żæģĖŁŃ¹ĖõÖĮ2L·ūŗĻ£»ĖłŅŌ“š°øŹĒ£ŗ¼ÓČė“߻ƼĮ£»½«ČŻĘ÷µÄĢå»żæģĖŁŃ¹ĖõÖĮ2L£®
”¾æ¼µć¾«Īö”æ½ā“š“ĖĢāµÄ¹Ų¼üŌŚÓŚĄķ½ā»ÆŃ§Ę½ŗāדĢ¬±¾ÖŹ¼°ĢŲÕ÷µÄĻą¹ŲÖŖŹ¶£¬ÕĘĪÕ»ÆŃ§Ę½ŗāדĢ¬µÄĢŲÕ÷£ŗ”°µČ”±¼“ VÕż=VÄę>0£»”°¶Æ”±¼“ŹĒ¶ÆĢ¬Ę½ŗā£¬Ę½ŗāŹ±·“Ó¦ČŌŌŚ½ųŠŠ£»”°¶Ø”±¼“·“Ó¦»ģŗĻĪļÖŠø÷×é·Ö°Ł·Öŗ¬Įæ²»±ä£»”°±ä”±¼“Ģõ¼žøÄ±ä£¬Ę½ŗā±»“ņĘĘ£¬²¢ŌŚŠĀµÄĢõ¼žĻĀ½ØĮ¢ŠĀµÄ»ÆŃ§Ę½ŗā£»ÓėĶ¾¾¶ĪŽ¹Ų£¬Ķā½ēĢõ¼ž²»±ä£¬æÉÄę·“Ó¦ĪŽĀŪŹĒ“ÓÕż·“Ó¦æŖŹ¼£¬»¹ŹĒ“ÓÄę·“Ó¦æŖŹ¼£¬¶¼æɽØĮ¢Ķ¬Ņ»Ę½ŗāדĢ¬£ØµČŠ§£©£®


 Źī¼Ł×÷Ņµŗ£Ńą³ö°ęÉēĻµĮŠ“š°ø
Źī¼Ł×÷Ņµŗ£Ńą³ö°ęÉēĻµĮŠ“š°ø ±¾ĶĮ½ĢøØÓ®ŌŚŹī¼Łøߊ§¼ŁĘŚ×Üø“Ļ°ŌĘÄĻæĘ¼¼³ö°ęÉēĻµĮŠ“š°ø
±¾ĶĮ½ĢøØÓ®ŌŚŹī¼Łøߊ§¼ŁĘŚ×Üø“Ļ°ŌĘÄĻæĘ¼¼³ö°ęÉēĻµĮŠ“š°ø Źī¼Ł×÷Ņµ±±¾©ŅÕŹõÓėæĘѧµē×Ó³ö°ęÉēĻµĮŠ“š°ø
Źī¼Ł×÷Ņµ±±¾©ŅÕŹõÓėæĘѧµē×Ó³ö°ęÉēĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æA”¢B”¢C”¢D¾łĪŖ֊ѧ»Æѧ³£¼ūµÄĪļÖŹ£¬ĖüĆĒ¼äµÄ·“Ó¦¹ŲĻµČēĶ¼ĖłŹ¾£®
£Ø1£©ČōAŹĒæÉČÜŠŌĒæ¼ī£¬BŹĒÕżŃĪ£¬D²»ČÜÓŚĻ”ĻõĖį£¬ŌņBµÄ»ÆѧŹ½ĪŖ £® ÓŠ¹Ų·“Ó¦µÄ»Æѧ±ä»ÆµÄ»Æѧ·½³ĢŹ½ĪŖ £®
£Ø2£©ČōBŹĒÕżŃĪ£¬D¼ČæÉČÜÓŚŃĪĖįÓÖæÉČÜÓŚNaOHČÜŅŗ£®¢ŁAŹĒNaHCO3Ź±£¬øĆ·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ£ŗ £®
¢ŚAŹĒŅ»ÖÖµ»ĘÉ«¹ĢĢ壬ĒŅAÓėBŅŌĪļÖŹµÄĮæÖ®±ČĪŖ2£ŗ1Ļą»ģŗĻŹ±£¬ĶĘÖŖBµÄ»ÆѧŹ½ĪŖ£ŗ £®
£Ø3£©ČōAŹĒĢ¼»ÆøĘ£ØCaC2£©£¬AÓėBµÄČÜŅŗ·“Ó¦Ź±Ö»Éś³ÉĘųĢåC”¢CaCO3ŗĶĖ®£»ŌņBµÄ»ÆѧŹ½ĪŖ £® 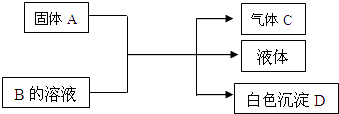
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æij¾§Ģå»ÆѧŹ½ĪŖN2H6SO4£¬Ę侧ĢåĄąŠĶÓėĮņĖįļ§ĻąĶ¬”£ŹŌ·ÖĪöŌŚøĆ¾§ĢåÖŠ²»»į“ęŌŚ£Ø £©
A.·Ö×Ó¼ä×÷ÓĆĮ¦B.¹²¼Ū¼üC.Ąė×Ó¼üD.ŃōĄė×Ó
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ¹čŹĒĪŽ»ś·Ē½šŹō²ÄĮĻµÄÖ÷½Ē£¬¹čµÄŃõ»ÆĪļŗĶ¹čĖįŃĪŌ¼Õ¼µŲæĒÖŹĮæµÄ90%ŅŌÉĻ”£
£Ø1£©ĻĀĮŠĪļÖŹ²»ŹōÓŚ¹čĖįŃĪµÄŹĒ£Ø____£©
A£®ĢÕ“É”””””””””””””” B£®²£Į§
C£®Ė®Äą D£®ÉśŹÆ»Ņ
£Ø2£©SiO2ŹĒ²£Į§µÄÖ÷ŅŖ³É·ÖÖ®Ņ»£¬SiO2ÓėĒāŃõ»ÆÄĘČÜŅŗ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ_______________________£¬¹¤ŅÕŹ¦³£ÓĆ________(ĢīĪļÖŹĆū³Ę)Ą“µńæĢ²£Į§”£
£Ø3£©Na2SiO3æÉĶعżSiO2Óė“æ¼ī»ģŗĻøßĪĀČŪČŚ·“Ó¦ÖĘµĆ£¬øßĪĀČŪČŚ“æ¼īŹ±ĻĀĮŠŪįŪöæÉŃ”ÓƵďĒ________”£
A£®ĘÕĶز£Į§ŪįŪö B£®ŹÆÓ¢²£Į§ŪįŪö
C£®Ńõ»ÆĀĮŪįŪö D£®ĢśŪįŪö
£Ø4£©¹¤ŅµÉĻ³£ĄūÓĆ·“Ó¦2C£«SiO2![]() Si£«2CO”üÖʱø¹čµ„ÖŹ£¬øĆ·“Ó¦ÖŠŃõ»Æ¼ĮŹĒ________”£
Si£«2CO”üÖʱø¹čµ„ÖŹ£¬øĆ·“Ó¦ÖŠŃõ»Æ¼ĮŹĒ________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æijČÜŅŗÖŠŗ¬ÓŠ½Ļ“óÅØ¶ČµÄH+”¢Fe2+”¢SO42-Ź±£¬ĻĀĮŠĪļÖŹæÉŅŌŌŚĘäÖŠ“óĮæ“ęŌŚµÄŹĒ
A.CuCl2B.Cl2 C.Ba(NO3)2D.ĀĮ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŹéŠ“ĻĀĮŠ·½³ĢŹ½£ŗ
£Ø1£©ŅŅĖįŗĶŅŅ“¼µÄõ„»Æ·“Ó¦·½³ĢŹ½
£Ø2£©¹¤ŅµŅ±Į¶Ć¾µÄ»Æѧ·½³ĢŹ½
£Ø3£©¶žŃõ»Æ¹čÓėĒā·śĖį»Æѧ·½³ĢŹ½
£Ø4£©Na2SO3ÓėFeCl3·“Ó¦µÄĄė×Ó·½³ĢŹ½
£Ø5£©»š·ØĮ¶Ķ»Æѧ·½³ĢŹ½ £®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŚČēĶ¼ĖłŹ¾µÄŅ»Š©³£¼ūĪļÖŹÖ®¼äµÄ×Ŗ»Æ¹ŲĻµÖŠ£ØÓŠŠ©·“Ó¦ÖŠµÄĖ®”¢²æ·Ö²śĪļ¼°·“Ó¦Ģõ¼žĪ“ĮŠ³ö£©”£

ŅŃÖŖ·“Ó¦¢ŁŹĒ¹¤ŅµÖĘĮņĖįŹ±·ŠĢŚĀÆÖŠµÄ·“Ó¦£¬AŹĒÓÉĮ½ÖÖŌŖĖŲ×é³ÉµÄ»ÆŗĻĪļĒŅŌŖĖŲµÄÖŹĮæ±ČĪŖ7£ŗ8£¬B”¢MĪŖ·Ē½šŹōµ„ÖŹ£¬E”¢KĪŖ½šŹōµ„ÖŹ£¬ĘäÖŠBĪŖµŲæĒÖŠŗ¬Įæ×ī¶ąµÄ·Ē½šŹōŌŖĖŲµÄµ„ÖŹ£¬EĪŖµŲæĒÖŠŗ¬Įæ×ī¶ąµÄ½šŹōŌŖĖŲµÄµ„ÖŹ”£
£Ø1£©MµÄ»ÆѧŹ½ĪŖ_________”£
£Ø2£©·“Ó¦¢ŁµÄ»Æѧ·½³ĢŹ½ĪŖ_________”£
£Ø3£©·“Ó¦¢ŚµÄ»Æѧ·½³ĢŹ½ĪŖ_________”£
£Ø4£©IµÄĖ®ČÜŅŗÓėK·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ_________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”潚Źōīę£ØĻ”ĶĮŌŖĖŲ£©ŠŌÖŹ»īĘĆ£®īę³£¼ūµÄ»ÆŗĻ¼ŪĪŖ+3ŗĶ+4£¬Ńõ»ÆŠŌ£ŗCe4+£¾Fe3+£¾I2 £® ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø £©
A.īęČÜÓŚĒāµāĖįµÄ»Æѧ·½³ĢŹ½æɱķŹ¾ĪŖ£ŗCe+4HIØTCeI4+2H2”ü
B.ÓĆCe£ØSO4£©2ČÜŅŗµĪ¶ØĮņĖįŃĒĢśČÜŅŗ£¬ĘäĄė×Ó·½³ĢŹ½ĪŖ£ŗCe4++Fe2+=Ce3++Fe3+
C.ŌŚŅ»¶ØĢõ¼žĻĀ£¬µē½āČŪȌדĢ¬µÄCeO2ÖĘCe£¬ŌŚŃō¼«»ńµĆīę
D.ĖÄÖÖīęµÄŗĖĖŲ ![]() Ce”¢
CeӢ ![]() CeӢ
CeӢ ![]() CeӢ
Ce”¢ ![]() Ce£¬ĖüĆĒ»„³ĘĪŖĶ¬ĖŲŅģŠĪĢå
Ce£¬ĖüĆĒ»„³ĘĪŖĶ¬ĖŲŅģŠĪĢå
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŃÖŖ£ŗŅŅ¶žĖį¾§ĢåČŪµć101.5”ę£»ŅŅ¶žĖį¾§Ģå¼ÓČČ·Ö½āµÄ·½³ĢŹ½ĪŖ£ŗH2C2O42H2O![]() 3H2O + CO2”ü+ CO”ü”£ĻÖĄūÓĆĻĀĮŠ×°ÖĆŃéÖ¤·“Ó¦²śĪļÖŠŗ¬ÓŠCO2ŗĶCO£Ø×°ÖĆ²»ÄÜÖŲø“Ź¹ÓĆ£©”£Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
3H2O + CO2”ü+ CO”ü”£ĻÖĄūÓĆĻĀĮŠ×°ÖĆŃéÖ¤·“Ó¦²śĪļÖŠŗ¬ÓŠCO2ŗĶCO£Ø×°ÖĆ²»ÄÜÖŲø“Ź¹ÓĆ£©”£Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ

£Ø1£©¼ģŃé×°ÖĆAĘųĆÜŠŌµÄ·½·ØŹĒ________________________________________________
£Ø2£©A×°ÖĆŹĒ·ńÓŠĪó_____________£ØĢī”°ŹĒ”±»ņ”°·ń”±£©£¬ŌŅņĪŖ_______________________
£Ø3£©°“ĘųĮ÷·½ĻņĮ¬½Óø÷ŅĒĘ÷£¬ÓĆŹż×Ö±ķŹ¾½ÓæŚµÄĮ¬½ÓĖ³Šņ£ŗ¢Ł”ś_________________________£»
£Ø4£©øĆĢ××°ÖĆÓŠĆ÷ĻŌȱĻŻ£¬ĒėÓčŅŌøüÕż________________________________________________
£Ø5£©Ö¤Ć÷CO“ęŌŚµÄŹµŃéĻÖĻóŹĒ_________________________________________________£»
£Ø6£©øł¾ŻĢāøųµÄŹż¾Ż£¬¼ŁÉč·“Ó¦²śÉśµÄĘųĢåČ«²æÅųö£¬²¢ÓėĪüŹÕŅŗ³ä·Ö·“Ó¦£ØĢįŹ¾£ŗB”¢CÖŠ³ĪĒåŹÆ»ŅĖ®¾łĻȱä»ė×Ē£¬ŗóÓÖ±ä³ĪĒ壩£¬×īÖÕDÖŠÉś³ÉĮĖĮ½ÖÖĪļÖŹ£¬ŌņÕāĮ½ÖÖÉś³ÉĪļµÄ»ÆѧŹ½¼°¶ŌÓ¦µÄĪļÖŹµÄĮæ·Ö±šŹĒ¢Ł_______________£¬¢Ś_______________”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com