
 ;
; ;
;| 催化剂 |
| △ |
| 引发剂 |
| 催化剂 |
| △ |
| 引发剂 |
 ;
; ,分子中有4种化学环境不同的H原子,其中甲基上1种,苯环上3种,故其一氯代物有4种,
,分子中有4种化学环境不同的H原子,其中甲基上1种,苯环上3种,故其一氯代物有4种,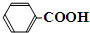 ;
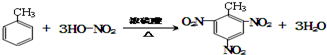
;
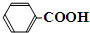 ;
; .
.


科目:高中化学 来源: 题型:
| A、烧杯、坩埚、试管、锥形瓶都可以用酒精灯直接加热 |
| B、银镜反应、乙醛与新制Cu(0H)2反应、实验室制取乙烯都必须用水浴加热 |
| C、制取氨气、氢气时都可以用向下排空气法收集 |
| D、石油的分馏、实验室制取乙炔和制取蒸馏水都要用到冷凝装置 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| n(Ca) |
| n(P) |
| n(Ca) |
| n(P) |

| n(Ca) |
| n(P) |
| PH值 | 6.8 | 7.2 | 8.0 | 9.0 | 10.0 | ||
| 产率(%) | 92.6 | 95.3 | 96.7 | 94.6 | 95.6 | ||
|
1.51 | 1.50 | 1.51 | 1.52 | 1.52 |
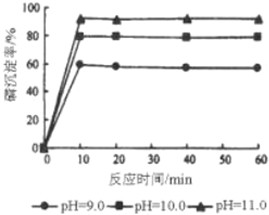
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 (1)氮元素是重要的非金属元素,可形成卤化物、氮化物、叠氮化物及配合物等多种化合物.
(1)氮元素是重要的非金属元素,可形成卤化物、氮化物、叠氮化物及配合物等多种化合物.| 晶格能/kJ?mol-1 | 熔点/℃ | |
| CaO | 3401 | 2927 |
| KCl | 699 | 772 |
| KBr | 689 | 734 |
| KI | 632 | 680 |

查看答案和解析>>
科目:高中化学 来源: 题型:
 (1)人们常用催化剂来选择反应进行的方向.如图所示为一定条件下1mol CH3OH与O2发生反应时,生成CO、CO2或HCHO的能量变化图[反应物O2(g)和生成物H2O(g)略去].
(1)人们常用催化剂来选择反应进行的方向.如图所示为一定条件下1mol CH3OH与O2发生反应时,生成CO、CO2或HCHO的能量变化图[反应物O2(g)和生成物H2O(g)略去].| 温度(℃) | 250 | 300 | 350 |
| K | 2.041 | 0.270 | 0.012 |
| 时间(min) | 5 | 10 | 15 | 20 | 25 | 30 |
| 压强比(P后/P前) | 0.98 | 0.90 | 0.80 | 0.70 | 0.70 | 0.70 |
| n(SO32-):n(HSO3-) | 91:9 | 1:1 | 1:91 |
| pH | 8.2 | 7.2 | 6.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、100mL0.5mol?L-1Mg(NO3)2溶液 |
| B、200mL1mol?L-1Ca(NO3)2溶液 |
| C、50mL1mol?L-1NaNO3溶液 |
| D、25mL0.5mol?L-1HNO3溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com