
【题目】图A所示的转化关系中(具体反应条件略),a、b、c和d分别为四种短周期元素的常见单质,其余均为它们的化合物,i的溶液为常见三大强酸,a的一种同素异形体的晶胞如图B(正四面体立体网状结构)所示. 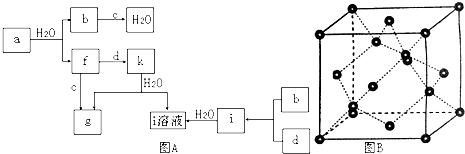
回答下列问题:
(1)图B对应的物质名称是 ,
(2)d中元素的原子核外电子排布式为 .
(3)图A中由二种元素组成的物质中,沸点最高的是 , 原因是 , 该物质的分子构型为 .
(4)图A中的双原子分子中,极性最大的分子是 .
(5)k的分子式为 , 中心原子的杂化轨道类型为 , 属于分子(填“极性”或“非极性”).
【答案】
(1)金刚石
(2)1s22s22p63s23p5
(3)H2O;分子间形成氢键; V型
(4)HCl
(5)COCl2; sp2;极性
【解析】解:a、b、c和d分别为四种短周期元素的常见单质,b与c反应生成水,故b、c分别为H2、O2中的一种,a的一种同素异形体的晶胞中每个原子周围有4个键,判断为金刚石,则a为C,故b为H2、c为O2,由转化关系可知,f为CO,g为CO2,因i是常见的三大强酸,只由b、d形成可判断为盐酸,则d为Cl2,i为HCl,而k与水反应生成CO2与盐酸,该反应没在教材中出现过,且由f、d反应得到,应含C、O、Cl三种元素,只能判断为COCl2.(1)有上述分析可知,图B对应的物质为金刚石,所以答案是:金刚石;(2)d中元素为Cl元素,基态原子电子排布式为:1s22s22p63s23p5,所以答案是:1s22s22p63s23p5;(3)所有两元素形成的物质中,水分子之间存在氢键,常温下是液态,其它都是气体,故水的沸点最高,水分子中O原子呈2个σ键、含有2对孤电子对,故为V型结构,
所以答案是:H2O;分子间形成氢键;V型;(4)所有双原子分子中,只有H、Cl电负性差值最大,因而HCl的极性最大,所以答案是:HCl;(5)k的分子式为COCl2,COCl2中C原子成3个σ键、1个π键,没有孤电子对,C原子采取sp2杂化,为平面三角形结构,分子中正负电荷中心不重合,属于极性分子,
所以答案是:COCl2;sp2;极性.


科目:高中化学 来源: 题型:
【题目】已知:pK=-lgK,25℃时,二元酸H2A的pK1=1.85,pK2=7.19。25℃时,用0.1mol/LNaOH溶液滴定20mL0.1mol/LH2A溶液的滴定曲线如图所示。下列说法正确的是

A. a点所得溶液中:Vo=10mL
B. C点所得溶液中:c(A2-)=c(HA-)
C. b点所得溶液中:c(H2A)+c(H+)=c(HA-)+c(OH-)
D. d点所得溶液中:A2-的水解平衡常数K1=1×10-7.19
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F、G均是原子序数小于36的元素.A的基态原子外围电子排布式为3s2;B原子的L电子层的P能级上有一个空轨道; C元素的基态原子最外层有3个未成对电子,次外层有2个电子; D 的原子的2p轨道上有1个电子的自旋方向与其它电子的自旋方向相反;E是海水中除氢、氧元素外含量最多的元素;F和G在周期表中既处于同一周期又位于同一族,且原子序数F比G小2. 根据信息回答下列问题:
(1)C的外围电子排布图为 . C与氢元素可分别形成含10个电子的分子、阴离子和阳离子,阳离子中中心原子的杂化类型为
(2)用电子式表示化合物AE2的形成过程
(3)F与BD易形成配合物F(BD)5 , 在F(BD)5中F的化合价为
(4)E有多种含氧酸根①EO﹣②EO2﹣③EO3﹣④EO4﹣ , 其中空间构型为四面体形的是(填序号).
(5)C 的最高价氧化物对应的水化物与A 的单质反应时,C被还原到最低价,该反应的化学方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有八种物质:①乙酸 ②苯 ③聚乙烯 ④苯酚 ⑤2-丁炔 ⑥甲醛 ⑦邻二甲苯 ⑧环己烯,既能使酸性高锰酸钾溶液褪色又能与溴水反应使之褪色的是
A. ①③④⑤⑧ B. ②④⑤⑦⑧ C. ④⑤⑥⑧ D. ③④⑤⑦⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镁、铝在生产生活中有广泛的应用.回答下列问题:
(1)铝的原子结构示意图为 . 它位于元素周期表的第周期,第族.
(2)实验室制备氢氧化铝的常用方法是在氯化铝溶液中滴加氨水,反应的离子方程式为 .
(3)常温下,铁跟水不反应,但红热的铁会跟水蒸气发生反应,反应的化学方程式为 .
(4)检验某溶液中是否含有Fe3+的操作方法是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】五种短周期主族元素W、M、X、X、Z原子序数依次增大,请结合表中信息回答下列问题:
元素 | W | M | X | Y | Z |
结构或性质 | 最高价含氧酸与其气态氢化物能发生化合反应 | 氢化物的水溶液能刻蚀玻璃 | 焰色反应呈火焰黄色 | 同周期主族元素形成的简单离子中,其离子半径最小 | 最高正价与最低负价代数和为6 |
(1)M元素在周期表中的位置为____________。
(2)M、X、Z元素所对应简单离子半径由大到小的顺序为__________(用离子符号表示)。
(3)W最高价含氧酸与其气态氢化物发生化合反应生成的物质中含有的化学键类型为_____。
(4)下列可作为比较M和Z的非金属性强弱的依据是_______(填序号)。
A.单质与H2反应的难易程度 B.氢化物的稳定性
C.最高价氧化物的水化物酸性强弱 D.将M的单质通入Z的钠盐溶液观察是否有Z逸出
(5)常温下,4.6gX单质在空中燃烧,再恢复到常温,放出QkJ能量,该反应的热化学方程式为_______________。
(6)W能形成多种氢化物,其中-种氢化物可作为火箭燃料,该物质中W与氢元素的质量比为7:1,写出该氢化物的电子式___________。该氢化物和O2在碱性条件下可形成燃料电池,产生两种无毒物质,写出其负极的电极反应式____________。
(7)Y元素和W元素形成的化合物YW一种新型无机材料,可与过量烧碱溶液反应产生使湿润的红色石蕊试纸变蓝的气体,写出有关的化学方程式___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有三组分散系:①四氯化碳和氯化钠溶液②碘酒③碘水,分离以上各混合液的主要方法依次是
A.分液、萃取、萃取B.萃取、蒸馏、分液
C.分液、蒸馏、萃取D.分液、萃取、蒸馏
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.胶体与溶液的本质区别在于是否具有丁达尔效应
B.电解质电离需要通电才能实现
C.只含有一种元素的物质一定是纯净物
D.向Fe(OH)3胶体中逐滴滴加稀硫酸,先出现沉淀,后来沉淀溶解
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com