


 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案科目:高中化学 来源: 题型:
| A、氢氧化铁溶于氢碘酸中:2Fe(OH)3+6H++2I-=2Fe2++I2+6H2O |
| B、明矾溶液中加入氢氧化钡溶液,使其产生沉淀的物质的量达最大值:Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+AlO2-+2H2O |
| C、Mg(HCO3)2溶液中加入过量石灰水:Mg2++2HCO3-+2Ca2++4OH-=2CaCO3↓+2H2O+Mg(OH)2↓ |
| D、向100mL 0.1mol/L的FeBr2溶液中通入0.012mol Cl2:10Fe2++14Br-+12Cl2=10Fe3++7Br2+24Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:
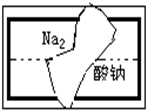 某研究性学习小组在整理实验室的化学试剂时,发现一盛有无色溶液的试剂瓶标签破损(如图),请你根据已掌握的知识,对该试剂可能是什么物质的溶液作出三种猜想,并设计实验验证,写出每一种猜想的实验操作、现象和结论.
某研究性学习小组在整理实验室的化学试剂时,发现一盛有无色溶液的试剂瓶标签破损(如图),请你根据已掌握的知识,对该试剂可能是什么物质的溶液作出三种猜想,并设计实验验证,写出每一种猜想的实验操作、现象和结论.| 猜想的化学物质 | 检验需要的试剂 | 操作、现象和结论 | |
| 1 | |||
| 2 | |||
| 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
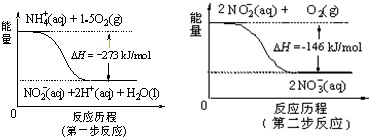
查看答案和解析>>
科目:高中化学 来源: 题型:
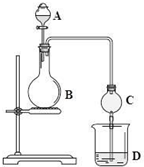 化学实验中,同一个装置可以用于不同的实验,例如图中的实验装置.(如图所示,B中可为固体或液体,可加热)
化学实验中,同一个装置可以用于不同的实验,例如图中的实验装置.(如图所示,B中可为固体或液体,可加热)查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com