
下列物质互为同分异构体的是( )
A.淀粉和纤维素
B.甘氨酸和硝基乙烷
C.醋酸和硬脂酸
D.甲醇和二甲醚
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
运用有关概念判断下列叙述正确的是( )
A.1molH2燃烧放出的热量为H2的燃烧热
B.Na2SO3和H2O2的反应为氧化还原反应
C.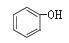 和
和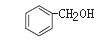 互为同系物
互为同系物
D.BaSO4的水溶液不导电,故BaSO4是弱电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
被称为“脑黄金”的DHA,是从深海鱼油中提取出的不饱和程度很高的脂肪酸,它的分子中有6个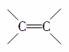 ,称为二十六碳六烯酸,则其甘油酯的分子结构简式为( )
,称为二十六碳六烯酸,则其甘油酯的分子结构简式为( )
A.(C25H51COO)3C3H5 B.(C25H39COO)3C3H5
C.(C26H41COO)3C3H5 D.(C26H47COO)3C3H5
查看答案和解析>>
科目:高中化学 来源: 题型:
某工厂废液经测定得知主要含有乙醇,其中还有丙酮、乙酸和乙酸乙酯,根据下表中各物质的性质,按下列步骤回收乙醇和乙酸。
| 物质 | 丙酮 | 乙酸乙酯 | 乙醇 | 乙酸 |
| 沸点/℃ | 56.2 | 77.06 | 78.5 | 117.9 |
①向废液中加入烧碱溶液,调整溶液的pH=10;②将混合液放入蒸馏器中缓缓加热;③收集温度在70℃~85℃时的馏出物;④排出蒸馏器中的残液,冷却后向其中加浓硫酸(过量),然后再放入耐酸蒸馏器中进行蒸馏,回收馏出物,请回答下列问题:
(1)加入烧碱使溶液的pH=10的目的是
________________________________________________________________________
________________________________________________________________________。
(2)在70℃~85℃时馏出物的主要成分是__________________。
(3)在步骤④中加入过量浓硫酸的目的是(用化学方程式表
示)________________________________________________________________________
________________________________________________________________________。
(4)当最后蒸馏的温度控制在85℃~125℃一段时间后,耐酸蒸馏器残液中溶质的主要成分是____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质中既能与盐酸反应,又能与NaOH溶液反应的是( )
①NaHCO3 ②(NH4)2S ③Al(OH)3 ④NH4Cl
⑤H2N—CH2—COOH ⑥CH3COOH
A.①②③ B.①②④⑤
C.⑤⑥ D.①②③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
亚硝酸(HNO2)是一种与醋酸酸性相当的弱酸,很不稳定,通常在室温下立即分解。
(1)在酸性条件下,当NaNO2与KI按物质的量1:1恰好完全反应,且I-被氧化为I2时,产物中含氮的物质为__________(填化学式)。
(2)要得到稳定的HNO2溶液,可以往冷冻的浓NaNO2溶液中加入或通入某种物质,下列物质不适合使用是_________(填序号)。
a.稀硫酸 b.二氧化碳 c.二氧化硫 d.磷酸
(3)工业废水中的NO2-可用铝粉除去.已知此反应体系中包含Al、NaAlO2、NaNO2、NaOH、NH3、H2O六种物质.将氧化剂和还原剂的化学式及其配平后的系数填入下列横线上:_________________________ + _________________________
上述反应后废水的pH值将________(填“增大”、“减小”或“不变”)。
(4)向20mL 0.01mol·L-1的NaNO2溶液中加入10mL 0.01 mol·L-1的AgNO3溶液,一段时间后,溶液中的c(Ag+)=________________________________。(已知:KSP(AgNO2)=2×10-8 mol2·L-2)
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:某温度时,KW=1.0×10-12。在该温度下,测得0.1mol·L-1Na2A溶液PH=6,则下列说法正确的是
A.H2A在水溶液中的电离方程式为:H2A=H++HA-,HA-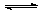 H++A2-
H++A2-
B.常温下,NH4HA溶液中滴加NaOH溶液至溶液pH=7,则c(Na+) = 2c(A2-)
C.相同条件下,体积相等、pH相等的盐酸与H2A溶液中和NaOH的量相等
D.0.0l mol·L-l的NaHA溶液pH>2
查看答案和解析>>
科目:高中化学 来源: 题型:
、三氟化氮(NF3)是无色无味气体,它可由氨气和氟气反应制得:4NH3+3F2===NF3+3NH4F。下列说法正确的是
A、NH4F的还原性比NH3强
B、NF3的氧化性比F2强
C、该反应中被氧化和被还原物质的物质的量之比为4∶3
D、该反应中得到1 mol NF3时,转移6 mol电子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com