
 ]
]
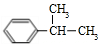 ,则A和B可以为:
,则A和B可以为: 或
或 ;A或B发生消去反应可得到C为
;A或B发生消去反应可得到C为 ,C与溴发生加成反应生成D为
,C与溴发生加成反应生成D为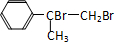 ,D发生水解反应生成E为
,D发生水解反应生成E为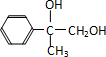 ,E发生催化氧化生成F为
,E发生催化氧化生成F为 ,F进一步发生氧化反应生成G为
,F进一步发生氧化反应生成G为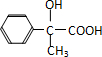 ,结合H的分子式可知,2分子G发生酯化反应生成H,则H为
,结合H的分子式可知,2分子G发生酯化反应生成H,则H为 ,G发生消去反应生成I,I发生加聚反应得到J,则I为
,G发生消去反应生成I,I发生加聚反应得到J,则I为 ,J为
,J为 ,据此解答.
,据此解答. ,则A和B可以为:
,则A和B可以为: 或
或 ;A或B发生消去反应可得到C为
;A或B发生消去反应可得到C为 ,C越溴发生加成反应生成D为
,C越溴发生加成反应生成D为 ,D发生水解反应生成E为
,D发生水解反应生成E为 ,E发生催化氧化生成F为
,E发生催化氧化生成F为 ,F进一步发生氧化反应生成G为
,F进一步发生氧化反应生成G为 ,结合H的分子式可知,2分子G发生酯化反应生成H,则H为
,结合H的分子式可知,2分子G发生酯化反应生成H,则H为 ,G发生消去反应生成I,I发生加聚反应得到J,则I为
,G发生消去反应生成I,I发生加聚反应得到J,则I为 ,J为
,J为 ,
, ,故答案为:
,故答案为: ;
; ,
, ;
; 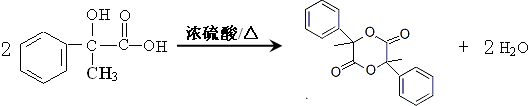 ,
, ;
;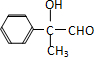 )的同分异构体的数目有6种:
)的同分异构体的数目有6种: 、
、 、
、 、
、 、
、 、
、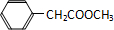 ,
, 等.
等.


科目:高中化学 来源: 题型:
| A、0.1mol/L |
| B、0.5 mol/L |
| C、0.01mol/L |
| D、0.05 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
 甲醇被称为2l世纪的新型燃料,工业上通过下列反应Ⅰ和Ⅱ,用CH4和H2O为原料来制备甲醇.
甲醇被称为2l世纪的新型燃料,工业上通过下列反应Ⅰ和Ⅱ,用CH4和H2O为原料来制备甲醇.| 实验编号 | T(℃) | n (CO)/n(H2) | P(MPa) | ||
| ⅰ | 150 |
| 0.1 | ||
| ⅱ | 5 | ||||
| ⅲ | 350 | 5 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、互为手性异构体的分子互为镜像,且分子组成相同,性质也相同 |
| B、由酸性FCH2COOH>CH3COOH,可知酸性ClCH2COOH>CH3COOH |
| C、由AgCl和AgBr都能溶于氨水中,而AgI不能溶解在氨水中,可知AgI在水中的溶解度更大 |
| D、除HF外,其他卤化氢沸点随相对分子质量增大而升高,是因为氢键的键能逐渐增大所致 |
查看答案和解析>>
科目:高中化学 来源: 题型:
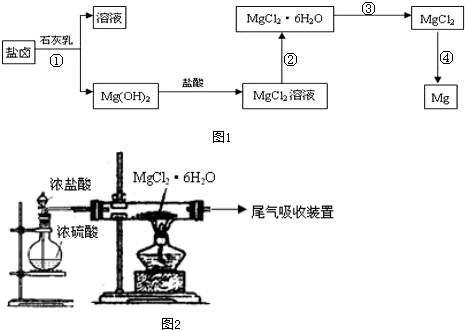
查看答案和解析>>
科目:高中化学 来源: 题型:
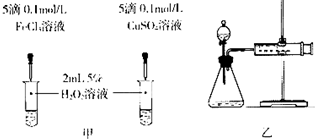
| 编号 | 操作 | 实验现象 |
| ① | 分别在试管A、B中加入5mL 5% H2O2溶液,各滴入2滴1mol/L FeCl3溶液.待试管中均有适量气泡出现时,将试管A放入盛有5℃左右冷水的烧杯中浸泡;将试管B放入盛有40℃左右热水的烧杯中浸泡. | 试管A中不再产生气泡; 试管B中产生的气泡量增大. |
| ② | 另取两支试管分别加入5mL 5% H2O2溶液和5mL 10% H2O2溶液 | 试管A、B中均未明显见到有 气泡产生. |
查看答案和解析>>
科目:高中化学 来源: 题型:
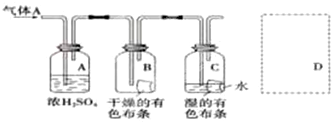
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验序号 | 甲 | 乙 | 丙 |
| 合金质量/m g | 255 | 385 | 459 |
| 生成气体体积/mL | 280 | 336 | 336 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com