
| A. | SiO2的用途广泛,主要用途是用于做半导体材料 | |
| B. | SiO2不与任何酸或碱性性氧化物反应 | |
| C. | SiO2和CO2的结构不同,但它们都具有氧化性,都能与强碱反应 | |
| D. | 因为高温时二氧化硅与碳酸钠反应放出CO2,所以硅酸的酸性比碳酸强 |
 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源: 题型:选择题
| A. | 苯(苯酚):加浓溴水,过滤 | |
| B. | 淀粉溶液(NaCl):半透膜,渗析 | |
| C. | 溴乙烷(乙醇):加蒸馏水,分液 | |
| D. | 乙酸乙酯(乙醇):加饱和碳酸钠溶液,分液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 ,关于它的叙述中正确的是( )
,关于它的叙述中正确的是( )| A. | 1mol该有机物最多能够和2molNaOH发生反应 | |
| B. | 和乙醇发生酯化反应时,羧基中的-OH将被CH3CH2-取代 | |
| C. | 铜做催化剂并加热的条件下,羟基中的氢氧键会断裂 | |
| D. | 和  互为同分异构体 互为同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 图为浓硫酸与铜片反应的装置.请回答:
图为浓硫酸与铜片反应的装置.请回答:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
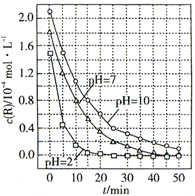
| A. | 溶液酸性越强,R的降解速率越小 | |
| B. | R的起始浓度越小,降解速率越大 | |
| C. | 在0~50 min之间,pH=2和pH=7时R的降解百分率相等 | |
| D. | 在20~25 min之间,pH=10时R的平均降解速率为0.02 mol•L-1•min-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2O2、NaClO中所含化学键类型完全相同 | |
| B. | 只有活泼金属与活泼非金属元素之间才能形成离子键 | |
| C. | D2O和T2O是同一物质 | |
| D. | 氯气与NaOH反应的过程中,同时又离子键、极性键和非极性键的断裂和形成 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯使溴的四氯化碳溶液褪色 | |
| B. | 乙烯使酸性KMnO4溶液褪色 | |
| C. | 将苯滴入溴水中,振荡后水层接近无色 | |
| D. | 甲烷与氯气混合,光照后黄绿色变浅 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 可能为甲烷和乙烷的混合物 | B. | 一定有乙烯 | ||
| C. | 混合物中可能含有丙烷 | D. | 两种气态烃一定都有四个H原子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com