
【题目】下列叙述正确的有( )
①需要通电才可以进行的有:电解、电离、电镀、电泳②水玻璃、福尔马林、天然橡胶、铝热剂都是混合物③![]() 、
、![]() 、
、![]() 均可由化合反应制得④油脂、淀粉、纤维素、天然橡胶都是天然有机高分子化合物⑤“血液透析”和“静电除尘”利用了胶体的同一种性质⑥
均可由化合反应制得④油脂、淀粉、纤维素、天然橡胶都是天然有机高分子化合物⑤“血液透析”和“静电除尘”利用了胶体的同一种性质⑥![]() 、
、![]() 分子中的碳原子均共面⑦铅蓄电池放电结束后,正极电极板的质量在减小
分子中的碳原子均共面⑦铅蓄电池放电结束后,正极电极板的质量在减小
A. 2个B. 3个C. 4个D. 5个
【答案】B
【解析】
①电离不需要通电,第①句话是错的;
②水玻璃是硅酸钠的水溶液,福尔马林是甲醛的水溶液,天然橡胶是聚合物,铝热剂是铝粉和金属氧化物的混合物,第②句话是正确的;
③![]() 可出
可出![]() 、
、![]() 、
、![]() 化合得到,
化合得到,![]() 可由
可由![]() 和
和![]() 化合得到,
化合得到,![]() 可出
可出![]() 、
、![]() 、
、![]() 化合得到,第③句话是正确的;
化合得到,第③句话是正确的;
④油脂不是高分子化合物,第④句话是错误的;
⑤血液和有粉尘的空气都是胶体,但两者利用的胶体性质是不同的,因此第⑤句话是错误的;⑥![]() 中甲基取代苯环中氢原子的位置,因此所有碳原子共面,
中甲基取代苯环中氢原子的位置,因此所有碳原子共面,![]() 中有三个碳碳双键,因此所有碳原子可以共面,第⑥句话是正确的;
中有三个碳碳双键,因此所有碳原子可以共面,第⑥句话是正确的;
⑦铅蓄电池放电时,生成的硫酸铅附着在电极板上,因此正极电极板的质量在增加,第⑦句话是错误的。
纵上所述,②③⑥正确,故选B。


 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案科目:高中化学 来源: 题型:
【题目】(1)研究有机物的方法有很多,常用的有①核磁共振氢谱②蒸馏③重结晶④萃取⑤红外光谱⑥过滤,其中用于分子结构确定的有____(填序号)。
(2)下列物质中,其核磁共振氢谱中只有一个吸收峰的是____(填字母)。
A.CH3CH3 B.CH3COOH
C.CH3COOCH3 D.CH3OCH3
(3)某含碳、氢、氧三种元素的有机物,经燃烧分析实验测定其碳的质量分数是64.86%,氢的质量分数是13.51%,则其实验式是________。如图是该有机物的质谱图,则其相对分子质量为______,分子式为________。
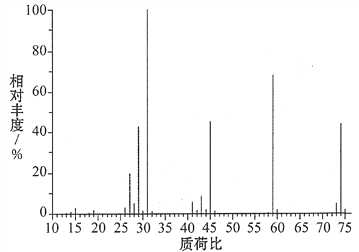
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,有![]() 的四种溶液:①
的四种溶液:①![]() ②
②![]() ③
③![]() ④
④![]()
(1)任选上述一种酸性溶液,用化学用语解释其呈酸性的原因:__________.
(2)溶液②的![]() _____________。
_____________。
(3)溶液②、③等体积混合后,溶液中![]() ________
________![]() (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
(4)溶液④加热后碱性增强,结合化学用语解释原因:______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaClO2 广泛用于造纸工业、污水处理等。工业上生产NaClO2 的工艺流程如下:

ClO2发生器中的反应为SO2 + 2NaClO3 + H2SO4 = 2ClO2↑+ 2NaHSO4
(1)NaClO3中Cl的化合价_______,上述反应中氧化剂是_______ ,被氧化的元素为_______。请用双线桥法表示该反应中电子转移的方向和数目SO2 + 2NaClO3 + H2SO4 = 2ClO2↑+ 2NaHSO4_______________________反应后,若产生0.6 mol气体,则电子转移的物质的量为 _______mol。
(2)吸收器中反应温度不能高于5℃的可能原因有 _______
(3)反应结束后,向ClO2发生器中通入一定量空气的目的是_______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知化学反应①:Fe(s)+CO2(g)![]() FeO(s)+CO(g),其化学平衡常数为K1;化学反应②:Fe(s)+H2O(g)
FeO(s)+CO(g),其化学平衡常数为K1;化学反应②:Fe(s)+H2O(g)![]() FeO(s)+H2(g),其化学平衡常数为K2,在温度973 K和1173 K的情况下,K1、K2的值分别如下:
FeO(s)+H2(g),其化学平衡常数为K2,在温度973 K和1173 K的情况下,K1、K2的值分别如下:
温度 | K1 | K2 |
973 K | 1.47 | 2.38 |
1 173 K | 2.15 | 1.67 |
(1)通过表格中的数值可以推断:反应①是_______(填“吸热”或“放热”)反应。
(2)现有反应③:CO2(g)+H2(g)![]() CO(g)+H2O(g),请你写出该反应的平衡常数K3的表达式:K3=______。
CO(g)+H2O(g),请你写出该反应的平衡常数K3的表达式:K3=______。
(3)根据反应①与②可推导出K1、K2与K3之间的关系式为__________,据此关系式及上表数据,能推断出反应③是________(填“吸热”或“放热”)反应。
(4)要使反应③在一定条件下建立的平衡向正反应方向移动,可采取的措施有______ 、_____ (填写字母序号)。
A.缩小反应容器的容积 B.扩大反应容器的容积
C.升高温度 D.使用合适的催化剂
E.设法减小平衡体系中的CO的浓度
(5)图甲、乙分别表示反应③在t1时刻达到平衡,在t2时刻因改变某个条件而发生变化的情况:

①图甲中t2时刻发生改变的条件是__________。
②图乙中t2时刻发生改变的条件是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求回答下列问题
(1)质子数为17、中子数为20的原子可表示为________,Na+的结构示意图________。
(2)焰色反应是_______变化,将碳酸钠进行焰色反应,火焰呈________。
(3)漂白粉有效成分的化学式________,漂白粉发挥漂白作用的反应方程式________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含氮化合物的种类非常丰富,请回答下列问题:
(1)已知:![]()
![]()
![]()
![]() 则
则![]()
![]() _____________。
_____________。
(2)![]() 温度时在容积为2L的恒容密闭容器中充入
温度时在容积为2L的恒容密闭容器中充入![]() 和
和![]() 发生反应:
发生反应:![]() ,
,![]() ,
,![]() 时达到平衡,此时
时达到平衡,此时![]() 转化率为80%,
转化率为80%,
①![]() 内该反应的平均速率
内该反应的平均速率![]() _____________;
_____________;
②![]() 温度时该反应的化学平衡常数
温度时该反应的化学平衡常数![]() ___________;
___________;
③若不改变外界条件,向平衡后的容器中再通入![]() ,重新达到平衡后,
,重新达到平衡后,![]() 在体系中的百分含量_____________。(填“变大”“变小”或“不变”)
在体系中的百分含量_____________。(填“变大”“变小”或“不变”)
(3)工业合成氨的反应原理为:![]() ,
,![]() 。对于该反应,既可以提高平衡体系中
。对于该反应,既可以提高平衡体系中![]() 的百分含量,又能加快反应速率的措施是(______)(填序号)
的百分含量,又能加快反应速率的措施是(______)(填序号)
a.升高温度 b.将平衡体系中的氨气分离出来 c.增大体系压强 d.加入合适的催化剂
(4)如图所示,![]() 温度时,
温度时,![]() 和
和![]() 的投料比与平衡时
的投料比与平衡时![]() 体积分数的关系。(不考虑
体积分数的关系。(不考虑![]() 与
与![]() 之间的相互转化)
之间的相互转化)

横坐标代表![]() 和
和![]() 的投料比,纵坐标代表平衡时
的投料比,纵坐标代表平衡时![]() 体积分数,计算最高点
体积分数,计算最高点![]() 时
时![]() 的平衡体积分数为_____________。
的平衡体积分数为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】体育竞技中服用兴奋剂既有失公平,也败坏了体育道德.某种兴奋剂的结构简式如图所示.有关该物质的说法中正确的是
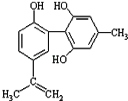
A.该物质与苯酚属于同系物,遇FeCl3溶液呈紫色
B.滴入酸性KMnO4溶液振荡,紫色褪去,能证明其结构中存在碳碳双键
C.该分子中的所有碳原子不可能共平面
D.1mol此物质分别与浓溴水和H2反应时最多消耗Br2和H2为4mol和7mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图中横坐标为加入反应物的物质的量,纵坐标为产生沉淀的物质的量。下列选项的编号和曲线的编号一一对应,其中描述错误的是
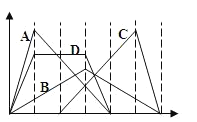
A. 向NaAlO2溶液中逐渐滴入HCl至过量
B. 向澄清石灰水中通入CO2至过量
C. 向含有盐酸的AlCl3溶液中滴入NaOH溶液至过量
D. 向含有等物质的量的Ca(OH)2、KOH的混合溶液中通入CO2至过量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com