
 ����������ز�Ʒ�����������Ӧ�ù㷺��
����������ز�Ʒ�����������Ӧ�ù㷺��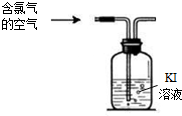
���� ��1��NaOH��Һ���ն�������������Ȼ��ơ��������ƺ�ˮ��
��2���������ܹ���Ӧ�����������ԣ��ܹ��뻹ԭ�����ʷ�����Ӧ�ݴ˽��
������������������Ӧ������������
��3���ٴ������ƾ���ǿ�������ԣ��ܹ��������������������ӣ�
������Һ��Ч�ɷ��Ǵ��������������̼��ˮ���ɵĴ����ᣬ������ȶ�������ֽ⣻
�۴�����������������ӷ���������ԭ��Ӧ����������ˮ��
��4������������ӷ���������ԭ��Ӧ�����ӷ���ʽ��Cl2+2I-=I2+2Cl-������100mL0.001mol•L-1KI��Һ��ͬʱ��������������$\frac{0.001��0.001}{2}$��71��103mg���ж��Ƿ꣬����Ҫ֪��ͨ��������������Ϊ�����������ĺ�������0.1 mg/m3�ͻ������ж���
��� �⣺��1�����������ж����壬��ʵ���ҽ������ʵ��ʱ�����������β��������β�����յ�ԭ������������������Һ���գ���Ӧ�Ļ�ѧ����ʽΪ��Cl2+2NaOH=NaCl+NaClO+H2O��
�ʴ�Ϊ��Cl2+2NaOH=NaCl+NaClO+H2O��
��2���������ܹ���Ӧ�����������ԣ��ܹ��뻹ԭ�����ʷ�����Ӧ�������ü������ʻ���ԭ���������գ�
a���Ȼ�����Һ����������Ӧ����a����
b���������������ԣ������������л�ԭ�ԣ��������ܹ�������������Ӧ���������ն������������b��ȷ��
c��Na2SO4��Һ���ܹ���������Ӧ��������������������c����
d��KMnO4��Һǿ�����ԣ���������ǿ�����ԣ����߲��ܷ�����Ӧ���������ն������������d����
��ѡb��
�ʴ�Ϊ��b��
��ѡ��������Լ���Cl2��Ӧ�����Ȼ���������������������Һ��Ӧ�����ӷ���ʽ��2Fe2++Cl2=2Fe3++2Cl-��
�ʴ�Ϊ��2Fe2++Cl2=2Fe3++2Cl-��
��3����NaClO����Ư�����ã�������NaClO�������ԣ����������л�ԭ�ԣ�������������ԭ��Ӧ���Խ�����ʴ��
�ʴ�Ϊ��NaClO��ǿ�����ԣ���һ��������н�ǿ��ԭ�ԣ�
������Һ��Ч�ɷ��Ǵ��������������̼��ˮ���ɵĴ����ᣬ������ȶ�������ֽ⣬����Ӧ���ܷⱣ�棻
�ʴ�Ϊ������Һ����Ч�ɷ�NaClO��������е�CO2���ã�ʹ����ʣ�
�۴�����������������ӷ���������ԭ��Ӧ����������ˮ�����ӷ���ʽ��Cl-+ClO-+2H+=Cl2��+H2O��
�ʴ�Ϊ��Cl-+ClO-+2H+=Cl2��+H2O��
��4������������ӷ���������ԭ��Ӧ�����ӷ���ʽ��Cl2+2I-=I2+2Cl-������100mL0.001mol•L-1KI��Һ��ͬʱ��������������$\frac{0.001��0.001}{2}$��71��103mg���ж��Ƿ꣬����Ҫ֪��ͨ��������������Ϊ�����������ĺ�������0.1 mg/m3�ͻ������ж���
�ʴ�Ϊ��ͨ������������
���� ���⿼�������������ʺ��й�������ԭ��Ӧ�����ӷ���ʽ����д����Ŀ�Ѷ��еȣ���Ϥ�������ʺ���ع����ǽ���ؼ���


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Ba��OH��2��Һ��ϡ���ᷴӦ��Ba2++SO42-�TBaSO4�� | |
| B�� | CaCO3����ᷴӦ��CaCO3+2H+�TCa2++H2O+CO2�� | |
| C�� | NaHCO3��Һ��NaOH��Һ��Ӧ��HCO3-+OH-�TCO32-+H2O | |
| D�� | Cu��FeCl3��Һ��Ӧ��Cu+Fe3+�TCu2++Fe2+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����ʯ��ˮ | B�� | ����̼������Һ | C�� | �Ȼ�����Һ | D�� | ���ᱵ��Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
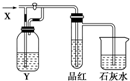 ��ͼ����һ�����������ʵ�ʵ��װ�ã���װ���л���ͨ������X�����رջ�������Ʒ����Һ�ޱ仯�������ʯ��ˮ����ǣ�����������Ʒ����Һ��ɫ���ݴ��ж�����X��ϴ��ƿ����ҺY�ֱ����Ϊ��������
��ͼ����һ�����������ʵ�ʵ��װ�ã���װ���л���ͨ������X�����رջ�������Ʒ����Һ�ޱ仯�������ʯ��ˮ����ǣ�����������Ʒ����Һ��ɫ���ݴ��ж�����X��ϴ��ƿ����ҺY�ֱ����Ϊ��������| A | B | C | D | |
| X | SO2 | SO2 | CO2 | Cl2 |
| Y | ���͵�NaHCO3��Һ | Ũ���� | Na2SO3 ��Һ | Na2CO3��Һ |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 0.32mol/��L•s�� | B�� | 0.16mol/��L•s�� | C�� | 0.8mol/��L•s�� | D�� | 0.08mol/��L•s�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | v��A��=0.45mol/��L•s�� | B�� | v��B��=0.6mol/��L•s�� | C�� | v��C��=0.5mol/��L•min�� | D�� | v��D��=0.4mol/��L•s�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
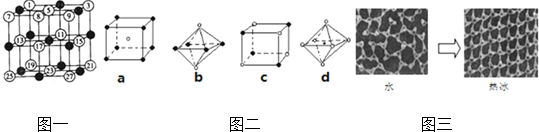
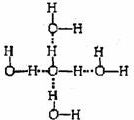
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ʵ������ȡ���� MnO2+4H++2Cl-$\frac{\underline{\;\;��\;\;}}{\;}$Mn2++Cl2��+2H2O | |
| B�� | �����İ�ˮ�μӵ��Ȼ�����Һ�� Al3++3NH3��H2O�TAl��OH��3��+3NH4+ | |
| C�� | ������ˮ��Ӧ��Cl2+H2O�TCl-+H++HClO | |
| D�� | С�մ���Һ�м������ʯ��ˮ2HCO3-+Ca2++2OH-�TCaCO3��+CO32-+2H2O |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com