
【题目】常温下,下列变化过程不是自发的是
A.石灰石的分解B.原电池产生电流
C.在密闭条件下体系从有序变为无序D.铁在潮湿空气中生锈
科目:高中化学 来源: 题型:
【题目】建构数学模型来研究化学问题,既直观又简洁。下列建构的数轴模型正确的是
A. 钠在氧气中燃烧,钠的氧化产物:
B. 铁在Cl2中燃烧,铁的氧化产物:![]()
C. NH3与Cl2反应,反应产物: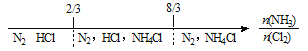
D. FeBr2溶液中通入Cl2,铁元素存在形式: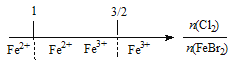
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,烧杯甲中盛有少量液态冰醋酸,烧杯乙中盛有NH4Cl晶体,在烧杯乙中再加入适量氢氧化钡晶体[Ba(OH)2·8H2O],搅拌,可观察到冰醋酸逐渐凝结为固体。下列有关判断正确的是( )

A. NH4Cl与Ba(OH)2·8H2O反应的焓变(ΔH)小于0
B. 反应物的总能量高于生成物的总能量
C. 反应中有热能转化为产物内部的能量
D. 反应中断裂的化学键只有离子键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有4瓶常用溶液:①BaCl2溶液,②NaCl溶液,③Na2SO4溶液,④CuSO4溶液。不用其他试剂,可通过实验方法将它们一一鉴别开来,鉴别出来的先后顺序可能是( )
A.④①②③B.④②①③C.④①③②D.①④③②
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将生铁炼成钢的主要目的是( )
A.适当增加生铁中碳的含量
B.除去铁中的碳、硫和磷
C.适当增加铁中硫和磷的含量
D.适当降低含碳量并除去大部分的硫和磷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种钌(Ru)基配合物光敏染料敏化太阳能电池的示意图如下。电池工作时电极上发生的反应为:
![]()
下列关于该电池的叙述正确的是
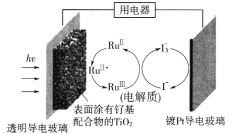
A. 电池工作时,是将化学能转化为电能
B. 电池工作时,电解质溶液中I-和I3-浓度不断减少
C. 透明导电玻璃上的电势比镀Pt导电玻璃上的电势高
D. 电解质溶液中发生反应:2Ru3++3I-=2Ru2++I3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用废铅蓄电池的铅泥(含PbSO4、PbO和Pb等)可制备精细化工产品3PbO·PbSO4·H2O(三盐),主要制备流程如下。
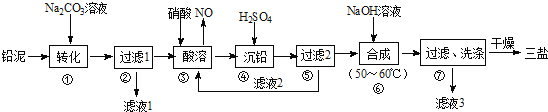
请回答下列问题:
(1)铅蓄电池在生活中有广泛应用,其工作原理是Pb+PbO2+2H2SO4![]() 2PbSO4+2H2O。若铅蓄电池放电前正、负极质量相等,放电时转移了1 mol电子,则理论上两极质量之差为__________。
2PbSO4+2H2O。若铅蓄电池放电前正、负极质量相等,放电时转移了1 mol电子,则理论上两极质量之差为__________。
(2)将滤液1、滤液3合并,经蒸发浓缩、降温结晶、过滤等操作,可得到一种结晶水合物(Mr=322),其化学式为______________________。
(3)步骤③酸溶时铅与硝酸反应生成Pb(NO3)2及NO。滤液2中溶质的主要成分为______(填化学式)。
(4)步骤⑥合成三盐的化学方程式为______________________。
(5)步骤⑦的洗涤操作中,检验沉淀是否洗涤完全的操作方法是__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度和压强下,在2 L的密闭容器中合成氨气:N2(g)+3H2(g)![]() 2NH3(g) 。在反应过程中反应物和生成物的物质的量随时间的变化如图所示。下列说法错误的是:
2NH3(g) 。在反应过程中反应物和生成物的物质的量随时间的变化如图所示。下列说法错误的是:
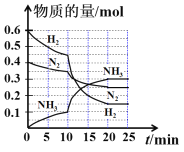
A. 0~10 min内,以NH3表示的平均反应速率为0.005 mol L-1 min-1
B. 10~20 min内,NH3浓度变化的原因可能是加入催化剂或缩小容器体积
C. 该反应在20 min时达到化学平衡状态
D. N2的平衡转化率与H2平衡转化率相等
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com