
 铜是常见的变价金属.为了比较正一价铜和正二价铜的稳定性,并研究氧化铜的氧化性,某化学小组的同学进行了以下实验.
铜是常见的变价金属.为了比较正一价铜和正二价铜的稳定性,并研究氧化铜的氧化性,某化学小组的同学进行了以下实验.分析 实验一、取一定量制得的氢氧化铜固体,于坩埚中灼烧,当温度达到80~100℃得到黑色固体粉末,继续加热至1000℃以上,黑色粉末全部变成红色粉末氧化亚铜,说明高温时,+1价的铜比+2价的铜稳定,取适量红色氧化亚铜粉末于洁净试管中,加入过量的稀硫酸(或盐酸),Cu2O+2H+=Cu2++Cu+H2O得到蓝色溶液,同时观察到试管底部还有红色固体存在,说明溶液中,+2价的铜比+1价的铜稳定.
(1)根据信息:氢氧化铜固体,于坩埚中灼烧,当温度达到80~100℃得到黑色固体粉末为氧化铜;继续加热至1000℃以上,黑色粉末全部变成红色粉末氧化亚铜,说明高温+1价铜稳定;
(2)根据信息:红色氧化亚铜粉末于洁净试管中,加入过量的稀硫酸(或盐酸),得到蓝色溶液为+2价的铜盐溶液,同时观察到试管底部还有红色固体存在为铜单质,据此书写化学方程式;
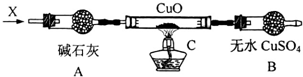
实验二、将X通入灼热的CuO燃烧管完全反应后,生成物中还有一种能使澄清石灰水变浑浊的气体Y应为二氧化碳,消耗0.01mol X,无水硫酸铜变成蓝色,测得B装置增重0.54g,即生成水0.03mol,并收集到0.88g气体Y即0.02molCO2,根据碳元素和氢元素守恒可知,某种气态烃(X)为C2H6,
(3)根据原子守恒确定气态氢化物的化学式,计算摩尔质量;
(4)根据实验现象来书写化学方程式;
解答 解:Ⅰ.问题1:铁和铜都有变价,具有相似点,正二价铁的稳定性小于正三价的铁,探究正一价铜的稳定性是否也小于正二价的铜,解决问题取一定量制得的氢氧化铜固体,于坩埚中灼烧,当温度达到80~100℃得到黑色固体粉末,继续加热至1000℃以上,黑色粉末全部变成红色粉末氧化亚铜,说明高温时,+1价的铜比+2价的铜稳定,取适量红色氧化亚铜粉末于洁净试管中,加入过量的稀硫酸(或盐酸),Cu2O+2H+=Cu2++Cu+H2O得到蓝色溶液,同时观察到试管底部还有红色固体存在,说明溶液中,+2价的铜比+1价的铜稳定.
(1)根据信息:氢氧化铜固体,于坩埚中灼烧,当温度达到80~100℃得到黑色固体粉末;继续加热至1000℃以上,黑色粉末全部变成红色粉末氧化亚铜,根据在不同温度下反应物的组成可确定物质的稳定性,所以高于1000℃时Cu2O比CuO稳定,在溶液中:Cu2O+2H+=Cu+Cu2++H2O,所以Cu2+比Cu+稳定,
故答案为:高温时,+1价的铜比+2价的铜稳定,而溶液中,+2价的铜比+1价的铜稳定;
(2)根据信息:红色氧化亚铜粉末于洁净试管中,加入过量的稀硫酸(或盐酸),得到蓝色溶液为+2价的铜盐溶液,同时观察到试管底部还有红色固体为铜单质,Cu2O中+1价的铜在酸性溶液中发生氧化还原反应:Cu2O+2H+=Cu+Cu2++H2O,
故答案为:Cu2O+2H+=Cu+Cu2++H2O;
实验二、将X通入灼热的CuO燃烧管完全反应后,生成物中还有一种能使澄清石灰水变浑浊的气体Y应为二氧化碳,消耗0.01mol X,无水硫酸铜变成蓝色,测得B装置增重0.54g,即生成水0.03mol,并收集到0.88g气体Y即0.02molCO2,根据碳元素和氢元素守恒可知,某种气态烃(X)为C2H6,
(3)根据上面的分析可知,X为C2H6,X气体其摩尔质量为30g/mol,
故答案为:30g/mol;
(4)C中发生反应的化学方程式为C2H6和氧化铜反应:7CuO+C2H6$\frac{\underline{\;\;△\;\;}}{\;}$7Cu+2CO2↑+3H2O,
故答案为:7CuO+C2H6$\frac{\underline{\;\;△\;\;}}{\;}$7Cu+2CO2↑+3H2O.
点评 本题考查实验探究和数据处理,做题时注意变价金属氧化物的性质以及质量守恒定律计算物质的化学式.题目难度中等.


 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 平衡不会发生移动 | B. | SO3的质量分数增大 | ||
| C. | 混合气体的密度减小 | D. | 混合气体的平均相对分子质量不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  用于Cu和浓H2SO4反应制取少量的SO2气体 | |
| B. |  用于分离水和苯的混合物 | |
| C. |  用于制备并收集NO2气体 | |
| D. |  用于除去碳酸氢钠固体中的少量碳酸钠 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2O2在①中是氧化剂,在②中是还原剂 | |
| B. | Mn2+在①中是还原产物,在②中是氧化产物 | |
| C. | 在①中每生成1 mol O2,转移的电子数为2.408×1024 | |
| D. | 在二氧化锰催化作用下1 mol H2O2分解生成0.5 mol O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 微粒的半径:Si>Mg | B. | 氧元素不存在同素异形体 | ||
| C. | Mg的还原性强于Si | D. | 该反应是置换反应,镁元素被氧化 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 苯甲酸苯酯是重要的有机合成中间体,工业上用二苯甲酮制备苯甲酸苯酯.
苯甲酸苯酯是重要的有机合成中间体,工业上用二苯甲酮制备苯甲酸苯酯.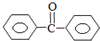 $→_{浓H_{2}SO_{4}、CH_{3}COOH}^{K_{2}S_{2}O_{8}}$
$→_{浓H_{2}SO_{4}、CH_{3}COOH}^{K_{2}S_{2}O_{8}}$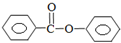
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com