
| A. | 都可以与水反应生成氢气和碱 | |
| B. | 都能从硫酸铜溶液中置换出铜 | |
| C. | 去除铝表面的铜镀层可以选用稀硝酸 | |
| D. | 铁丝不论在空气中还是在纯氧中都可以发生氧化还原反应 |
分析 A.活泼金属和水反应生成碱和氢气,铁和水蒸气反应生成四氧化三铁和氢气;
B.活泼金属和盐溶液反应,先和水反应生成碱和氢气,生成的碱再和盐发生反应;
C.铝和铜、铝都能发生反应;
D.铁丝在纯氧中燃烧生成四氧化三铁,铁丝在空气中潮湿的空气中形成原电池反应,表面生锈;
解答 解:A.活泼金属钠和水反应生成碱和氢气,铝和水加热反应生成氢氧化铝和氢气,铁和水蒸气反应生成四氧化三铁和氢气,3Fe+4H2O$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2,故A错误;
B.铝、铁可以置换硫酸铜溶液中的铜,活泼金属钠和盐溶液反应,先和水反应生成氢氧化钠和氢气,生成的氢氧化钠和硫酸铜发生反应,生成氢氧化铜沉淀,不能置换出铜,故B错误;
C.铝和铜、铝都能发生反应,去除铝表面的铜镀层可以选用浓硝酸,能溶解铜,铝在浓硝酸中发生钝化,不能继续反应,故C错误;
D.铁丝在纯氧中燃烧生成四氧化三铁,铁丝在空气中潮湿的空气中形成原电池反应,铁做负极被氧化表面生锈,反应过程中都是铁元素化合价升高做还原剂被氧化,发生氧化反应,故D正确;
故选D.
点评 本题考查了金属性质,主要是金属和水、和酸、和盐反应的规律和不同,掌握基础是解题关键,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | Ca(OH)═Ca2++2OH- | B. | KNO3═K++NO3- | C. | NH4Cl═4NH++Cl- | D. | H2SO4═2H++SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用乙烷和氯气混合光照充分反应,可以制得比较纯净的氯乙烷 | |
| B. | 可以用质谱仪快速、微量、精确地测定它的相对分子质量 | |
| C. | 与其它卤代烃一样,不溶于水,能溶于有机溶剂 | |
| D. | 它在氢氧化钠水溶液中,可以水解发生取代反应,生成乙醇 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
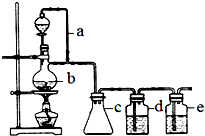 某研究性学习小组为合成1-丁醇,查阅资料得知一条合成路线:
某研究性学习小组为合成1-丁醇,查阅资料得知一条合成路线:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | KClO3 | B. | KMnO4 | C. | MnO2 | D. | Ca(ClO)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
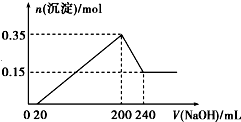
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
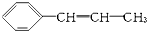 ,它可能具有的性质是( )
,它可能具有的性质是( )| A. | 易溶于水,也易溶于有机溶剂 | |
| B. | 既能使溴水褪色,又能使酸性KMnO4溶液褪色 | |
| C. | 能发生聚合反应,其产物可表示为 | |
| D. | 能使溴水褪色,但不能使酸性KMnO4溶液褪色 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com